1. Карно процесі. Термодинамикада көптеген дөңгелек процестердің ішінде Карно процесінің маңызы өте зор. Бұл процесс жүйенің күйін температуралары тұрақты 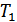 және
және 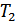 болатын екі жылу резервуарларымен жылулық жанастыру арқылы өзгертуге болатын квазистатикалық процесс болып табылады. Карно циклімен жұмыс жасайтын жылу машинасы идеал жылу машинасы болып табылады. Карно циклі былай жүреді. Жүйе температурасы
болатын екі жылу резервуарларымен жылулық жанастыру арқылы өзгертуге болатын квазистатикалық процесс болып табылады. Карно циклімен жұмыс жасайтын жылу машинасы идеал жылу машинасы болып табылады. Карно циклі былай жүреді. Жүйе температурасы 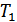 қыздырғышпен жылулық жанастырылады. Одан кейін
қыздырғышпен жылулық жанастырылады. Одан кейін
| P |
| V |
| 1 |
| V2 |
| V1 |
| 0 |
| 28-сурет. |
| 3 |
| 2 |
| 4 |
| V3 |
| V4 |
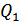 жылу мөлшерін алып, сыртқы күштерге қарсы
жылу мөлшерін алып, сыртқы күштерге қарсы 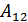 жұмысын атқарады. Енді жүйе адиабаталық оқшауланып 2-3 адиабата бойымен температурасы суытқыштың
жұмысын атқарады. Енді жүйе адиабаталық оқшауланып 2-3 адиабата бойымен температурасы суытқыштың 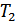 температурасымен теңелгенше квази-статикалық ұлғаяды. Адиабаталық ұлғаю кезінде жүйе сыртқы қысымға қарсы
температурасымен теңелгенше квази-статикалық ұлғаяды. Адиабаталық ұлғаю кезінде жүйе сыртқы қысымға қарсы 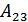 жұмысын атқарады. Жүйе 3 -күйде суытқышпен жанастырылып, сыртқы қысымды үздіксіз арттыру есебінен тұрақты
жұмысын атқарады. Жүйе 3 -күйде суытқышпен жанастырылып, сыртқы қысымды үздіксіз арттыру есебінен тұрақты 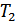 температурада квазистатикалық сығылады да 4- күйіне келеді. Бұл процесте жүйе суытқышқа
температурада квазистатикалық сығылады да 4- күйіне келеді. Бұл процесте жүйе суытқышқа 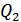 жылу мөлшерін береді. 4 -күйі осы күйден бастапқы 1- күйге адиабаталық квазистатикалық сығылып өтуге болатындай таңдап алынады. 3-4 изотермиялық сығылу процесі кезінде жүйе үстінен
жылу мөлшерін береді. 4 -күйі осы күйден бастапқы 1- күйге адиабаталық квазистатикалық сығылып өтуге болатындай таңдап алынады. 3-4 изотермиялық сығылу процесі кезінде жүйе үстінен 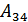 жұмысы атқарылады. Бұл жұмысты жүйенің теріс жұмысы деп те қарастыруға болады. Жүйе бастапқы күйіне оралуы үшін оны адиабаталық сығамыз. Бұл процесс кезіндегі
жұмысы атқарылады. Бұл жұмысты жүйенің теріс жұмысы деп те қарастыруға болады. Жүйе бастапқы күйіне оралуы үшін оны адиабаталық сығамыз. Бұл процесс кезіндегі 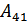 жұмысы да жүйе үстінен атқарылғандықтан теріс мәнге ие болады.
жұмысы да жүйе үстінен атқарылғандықтан теріс мәнге ие болады. 2. Карно циклінің ПӘК-і. Кез келген жүйенің пайдалы әсер коэффициенті (ПӘК-і)мына формуламен анықталатындығы белгілі:
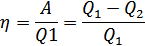
мұндағы 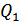 -жүйенің қыздырғыштан алған жылу мөлшері,
-жүйенің қыздырғыштан алған жылу мөлшері, 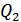 -жүйенің суытқышқа беретін жылу мөлшері, ал
-жүйенің суытқышқа беретін жылу мөлшері, ал 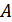 -жүйенің атқарған пайдалы жұмысы. Осы пайдалы жұмыс жүйенің толық бір циклі ішінде атқарған жұмыстарының қосындысына тең болады:
-жүйенің атқарған пайдалы жұмысы. Осы пайдалы жұмыс жүйенің толық бір циклі ішінде атқарған жұмыстарының қосындысына тең болады:
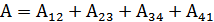 (35.1)
(35.1)
Екінші жағынан бұл жұмыс ПӘК формуласына сәйкес:
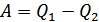 ,
,
демек
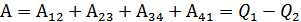
Енді осы жұмыстарды жеке-жеке қарастырайық.
1) 1-2 процесі - 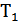 температурасында изотермиялық ұлғаю процесі болып табылады, бұл процесте жүйе көлемі
температурасында изотермиялық ұлғаю процесі болып табылады, бұл процесте жүйе көлемі 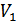 -ден
-ден 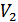 -ге дейін ұлғаяды. Демек,
-ге дейін ұлғаяды. Демек, 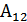 жұмысын былай анықтаймыз:
жұмысын былай анықтаймыз:
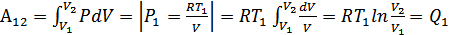 (35.2)
(35.2)
2) 2-3 процесі кезінде жүйе адиабаталық 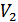 -ден
-ден 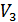 -ке дейін ұлғаяды, ал температурасы
-ке дейін ұлғаяды, ал температурасы 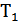 -ден
-ден 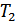 -ге дейін азаяды. Бұл процеске адиабата теңдеуін қолданамыз:
-ге дейін азаяды. Бұл процеске адиабата теңдеуін қолданамыз:
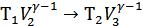
Бұдан
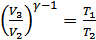 . (35.3)
. (35.3)
Сондықтан
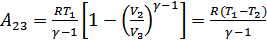 (35.4)
(35.4)
3) 3-4 процесі 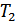 температурада изотермиялық
температурада изотермиялық 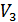 -ден
-ден 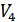 -ке дейін сығылу процесі болып табылады. Бұл процесте жүйе суытқышқа
-ке дейін сығылу процесі болып табылады. Бұл процесте жүйе суытқышқа 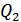 жылу мөлшерін береді. Ал
жылу мөлшерін береді. Ал 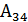 жұмысын былай анықтаймыз:
жұмысын былай анықтаймыз:
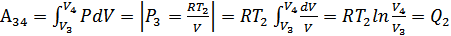 (35.5)
(35.5)
4) 4-1 процесі 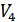 -тен
-тен 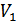 -ге дейін адиабаталық сығылуға сәйкес келеді. Бұл процесс кезінде жүйенің температурасы
-ге дейін адиабаталық сығылуға сәйкес келеді. Бұл процесс кезінде жүйенің температурасы 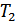 -ден
-ден 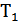 -ге дейін артады.Бұл процеске адиабата теңдеуін қолдансақ:
-ге дейін артады.Бұл процеске адиабата теңдеуін қолдансақ:
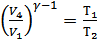 (35.6)
(35.6)
Осы процесте атқарылған жұмысты былай анықтаймыз:
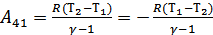 (35.7)
(35.7)
Осымен газ бастапқы күйге қайтып келеді. Карно циклі аяқталып, газ жаңа процесті бастауға дайын. Осы бір цикл ішінде атқарылған пайдалы жұмысты анықтайық:
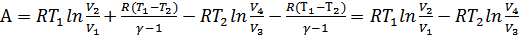 .
.
Осы жұмысты анықтау үшін (35.3) және (35.6) өрнектерді салыстырайық. Олардың оң жақтары бір-біріне тең, олай болса:
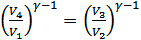 ,
,
демек,
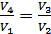 ,
,
бұдан
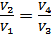 ,
,
Соңғы өрнекті қолдансақ, онда толық жұмыс:
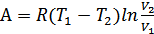 . (35.8)
. (35.8)
Енді Карно процесінің ПӘК-ін анықтайық. 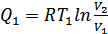 екендігін жоғарыда анықтағанбыз.
екендігін жоғарыда анықтағанбыз.
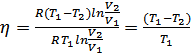 .
.
немесе
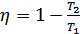 (35.9)
(35.9)
Осы формуладан Карно циклімен жұмыс жасайтын жылу машинасының ПӘК-і тек қана 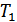 және
және 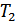 температураларға тәуелді екендігін көреміз.
температураларға тәуелді екендігін көреміз.
3. Карно принципі және теоремалары. Карно принципіне сәйкес циклді жылу машинасының жұмыс атқару процесінде температуралары әртүрлі екі дене (қыздырғыш пен суытқыш) міндетті түрде қатысуы керек.
Карноның 1-теоремасы: Қыздырғыш пен суытқыштың берілген тұрақты температураларында жұмыс істейтін кез келген жылу машинасының ПӘК-і қыздырғыш пен суытқыштың сондай температураларында қайтымды Карно циклімен жұмыс істейтін идеал жылу машинасының ПӘК-інен артық болуы мүмкін емес.
Карноның 2-теоремасы: Карно циклімен жұмыс істейтін идеал жылу машинасының пайдалы әсер коэффициенті тек қана қыздырғыш 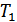 пен суытқыштың
пен суытқыштың 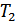 температураларына тәуелді, ал машинаның құрылымына және жұмыстық дененің түріне тәуелді емес.
температураларына тәуелді, ал машинаның құрылымына және жұмыстық дененің түріне тәуелді емес.
Карноның бірінші теоремасына сәйкес 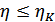 теңсіздігі орындалады. Мұндағы
теңсіздігі орындалады. Мұндағы 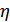 -кез келген жылу машинасының ПӘК-і, ал
-кез келген жылу машинасының ПӘК-і, ал 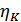 -Карно циклімен жұмыс жасайтын идеал жылу машинасының ПӘК-і. Олай болса мынадай теңсіздік орындалуы керек:
-Карно циклімен жұмыс жасайтын идеал жылу машинасының ПӘК-і. Олай болса мынадай теңсіздік орындалуы керек:
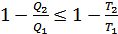 . (35.10)
. (35.10)
Бұл өрнекті түрлендірсек мынадай қатынас аламыз:
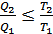 (35.11)
(35.11)
Егер жүйенің алған жылу мөлшерін 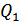 оң деп ескерсек, онда жүйенің берген жылу мөлшері
оң деп ескерсек, онда жүйенің берген жылу мөлшері 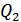 теріс болады. Осыларды ескерсек (35.11) өрнекті былай жазуға болады:
теріс болады. Осыларды ескерсек (35.11) өрнекті былай жазуға болады:
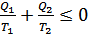 . (35.12)
. (35.12)
немесе, осы дөңгелек процесс үшін
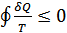 (35.13)
(35.13)
болады. Бұл қатынасты Клаузиус теңсіздігі деп атайды.
Бақылау сұрақтары:
1. Карно циклінде қандай процестер тізбегі өтеді?
2. Карно циклінің ПӘК-ін қорытып шығарыңыз.
3. Карно циклінің ПӘК-і қандай шамаларға тәуелді?
4. ПӘК-і Карно циклінің ПӘК-інен артық жылу машинасын жасауға бола ма?
5. Карно циклі дәл қайтымды процеске жата ма?
§36. Температураның термодинамикалық шкаласы
1. 1848 жылы Вильям Томсон (Лорд Кельвин) Карно теоремасын қолданып, термометрлік дененің (заттың) қасиеттерінің ерекшеліктеріне және термометрдің құрылымына тәуелді емес рационалды температуралық шкала құруға болатынын көрсетті. Карно теоремасы бойынша Карно циклінің ПӘК-і тек қыздырғышпен суытқыштың температураларына тәуелді. Қандай да бір термометрмен өлшенген қыздырғыш пен суытқыштың эмпирикалық температураларын 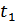 және
және 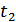 деп белгілейік. Онда
деп белгілейік. Онда
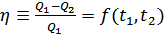 (36.1)
(36.1)
мұндағы 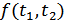 - таңдалған
- таңдалған 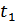 және
және 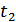 эмпирикалық температуралардың универсал функциясы. Бұл функцияның түрі Карно машинасының құрылымына және жұмыстық денесіне тәуелді емес.
эмпирикалық температуралардың универсал функциясы. Бұл функцияның түрі Карно машинасының құрылымына және жұмыстық денесіне тәуелді емес.
2. Температураның термодинамикалық шкаласын құру үшін 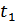 және
және 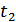 температураларының қарапайым функциясын қарастырамыз:
температураларының қарапайым функциясын қарастырамыз:
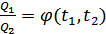 . (36.2)
. (36.2)
| P |
| V |
| 1 |
| 0 |
| 29-сурет. |
| 3 |
| 2 |
| 4 |
| 5 |
| 6 |
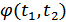 -функциясы
-функциясы 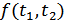 -функциясы арқылы оңай сипатталады.
-функциясы арқылы оңай сипатталады. 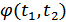 -функциясының жалпы түрін анықтайық. Ол үшін температуралары тұрақты үш жылулық резервуарды қарастырайық. Бұл резервуарлардың эмпирикалық темпера-тураларын сәйкесінше
-функциясының жалпы түрін анықтайық. Ол үшін температуралары тұрақты үш жылулық резервуарды қарастырайық. Бұл резервуарлардың эмпирикалық темпера-тураларын сәйкесінше 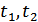 және
және 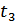 деп белгілейік. Осы резервуаларды суытқыш және қыздырғыш ретінде қолданып үш Карно циклін жүргіземіз (29-сурет).
деп белгілейік. Осы резервуаларды суытқыш және қыздырғыш ретінде қолданып үш Карно циклін жүргіземіз (29-сурет). 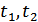 және
және 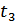 температуралары 1-2, 4-3, 6-5 изотермаларына сәйкес келсін. 1-2-3-4 және 4-3-5-6 Карно циклдері үшін
температуралары 1-2, 4-3, 6-5 изотермаларына сәйкес келсін. 1-2-3-4 және 4-3-5-6 Карно циклдері үшін 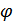 функциясын былай анықтауға болады:
функциясын былай анықтауға болады: 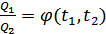 ,
, 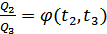 .
.
Осы екі теңдеуді бірге шешсек, онда:
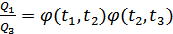 .
.
Біз 1-2-5-6 Карно циклін сипаттайтын өрнекті алдық. Демек, 1-2-3-4 және 4-3-5-6 Карно циклдері 1-2-5-6 циклін береді. Себебі, бұл екі циклде біз 4-3 изотермасын оң және теріс бағыттарда өттік, сондықтан бұл изотерманы қарастырмауға болады. Сонымен,
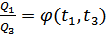 .
.
Соңғы екі өрнекті салыстырсақ,
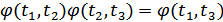 , (36.3)
, (36.3)
бұдан
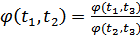 , (36.4)
, (36.4)
немесе
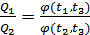 . (36.5)
. (36.5)
Бұл қатынас 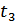 аргументінің кез келген мәні үшін дұрыс болады. Себебі теңдіктің сол жағы
аргументінің кез келген мәні үшін дұрыс болады. Себебі теңдіктің сол жағы 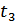 температурасына тәуелді емес. Егер
температурасына тәуелді емес. Егер 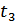 аргументін тұрақты етіп тағайындасақ, онда
аргументін тұрақты етіп тағайындасақ, онда 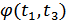 функциясын
функциясын 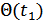 функциясымен алмастыра аламыз.
функциясымен алмастыра аламыз. 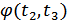 функциясы сәйкесінше
функциясы сәйкесінше 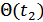 функциясымен алмастырылады. Олай болса,
функциясымен алмастырылады. Олай болса,
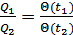 (36.6)
(36.6)
Сонымен 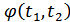 функциясы
функциясы 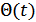 функциясының
функциясының 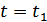 және
және 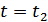 болғандағы мәндерінің қатынасы болып табылады.
болғандағы мәндерінің қатынасы болып табылады. 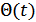 шамасы тек қана температураға тәуелді болғандықтан, оны дененің температурасының өлшемі ретінде қабылдауға болады.
шамасы тек қана температураға тәуелді болғандықтан, оны дененің температурасының өлшемі ретінде қабылдауға болады. 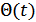 шамасын абсолюттік термодинамикалық температура деп атайды.
шамасын абсолюттік термодинамикалық температура деп атайды.
3. 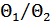 қатынасын эксперимент жүзінде анықтауға болады. Ол үшін
қатынасын эксперимент жүзінде анықтауға болады. Ол үшін 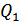 және
және 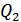 жылу мөлшерлерін өлшеу қажет, алайда жылу мөлшерлерінің қатынасы
жылу мөлшерлерін өлшеу қажет, алайда жылу мөлшерлерінің қатынасы 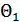 және
және 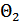 температураларын бір мәнді анықтамайды. Себебі,
температураларын бір мәнді анықтамайды. Себебі, 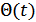 функциясы
функциясы 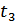 параметріне тәуелді, ал (36.6) өрнегі
параметріне тәуелді, ал (36.6) өрнегі 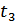 параметріне тәуелді емес.
параметріне тәуелді емес. 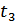 параметрінің таңдалған мәніне қарай термодинамикалық температуралардың мәні де әртүрлі болады. Термодинамикалық температураны бірмәнді анықтаудың екі жолы бар:
параметрінің таңдалған мәніне қарай термодинамикалық температуралардың мәні де әртүрлі болады. Термодинамикалық температураны бірмәнді анықтаудың екі жолы бар:
Біріншіден, қандай да бір екі температуралық нүктені аламыз. Мысалы, мұздың балқуының қалыпты нүктесі және судың қайнауының қалыпты нүктесі. Бұл температуралық нүктелерді 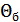 және
және 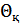 деп, ал оларға сәйкес Карно цикліндегі жылу мөлшерлерін
деп, ал оларға сәйкес Карно цикліндегі жылу мөлшерлерін 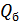 және
және 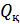 деп белгілейміз. Сондай-ақ,
деп белгілейміз. Сондай-ақ, 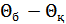 екі температура айырымын 100 градусқа тең деп қабылдаймыз. Сонымен, екі температуралық нүкте арасындағы интервал теңдей 100 бөлікке бөлінеді және оның әрқайсысы 1 Кельвинге тең. Енді (36.6) қатынасын мына түрде жазамыз:
екі температура айырымын 100 градусқа тең деп қабылдаймыз. Сонымен, екі температуралық нүкте арасындағы интервал теңдей 100 бөлікке бөлінеді және оның әрқайсысы 1 Кельвинге тең. Енді (36.6) қатынасын мына түрде жазамыз:
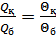 ,
, 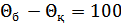 (36.7)
(36.7)
Бұл қатынастардан 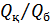 қатынасын экспериментте өлшеу арқылы
қатынасын экспериментте өлшеу арқылы 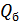 және
және 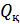 температураларын анықтауға болады. Нақты тәжірибелерде бұл қатынас өлшенбеген, бірақ бөгде өлшеулер нәтижесінде
температураларын анықтауға болады. Нақты тәжірибелерде бұл қатынас өлшенбеген, бірақ бөгде өлшеулер нәтижесінде 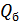 және
және 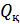 температуралары былай анықталған:
температуралары былай анықталған:
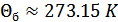 ,
, 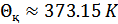 .(36.8)
.(36.8)
Кез келген дененің 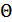 температурасын мынадай формула бойынша анықтауға болады:
температурасын мынадай формула бойынша анықтауға болады:
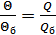 , (36.9)
, (36.9)
Ол үшін дене мен еріп жатқан мұз арасында Карно циклін жүргізіп 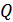 және
және 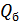 жылу мөлшерлерін өлшеу керек. Осылай құрылған шкала температураның абсолюттік термодинамикалық шкаласы деп аталады.Бұл бізге белгілі (§3) екі реперлік нүкте бойынша температура шкаласын жасау әдісі болып табылады.
жылу мөлшерлерін өлшеу керек. Осылай құрылған шкала температураның абсолюттік термодинамикалық шкаласы деп аталады.Бұл бізге белгілі (§3) екі реперлік нүкте бойынша температура шкаласын жасау әдісі болып табылады.
Екіншіден, температуралық шкаланы бір ғана реперлік нүкте бойынша, яғни бір температуралық нүкте бойынша жасауға болады. Мұндай нүкте ретінде судың үштік нүктесін алуға болады. Себебі, судың қалыпты қайнау температурасын 0,002-0,01 ºС дәлдігімен, мұздың қалыпты балқу температурасын 0,0002-0,001 ºС дәлдігімен қайталауға болады, ал судың үштік нүктесін арнайы құралдар көмегімен 0,0001 ºС дәлдігімен өлшеуге болады. Осыларды ескеріп 1954 ж. «Өлшемдер бойынша 10-шы генералдық конференцияның» шешімі бойынша температураның абсолюттік термодинамикалық шкаласын бір реперлік нүкте бойынша, дәлірек айтқанда судың үштік нүктесі бойынша жасау бекітілген. Сондай-ақ, үштік нүктенің температурасының мәні 273,16 К деп анықталған.
Бақылау сұрақтары:
1. Вильям Томсонның (Лорд Кельвин) термодинамикалық температура шкаласын жасау принципін түсіндіріңіз.
2. Термодинамикалық температура шкаласын жасауда неліктен судың үштік нүктесі алынған?
3. Судың қалыпты қайнау және мұздың қалыпты балқу температуралары қандай дәлдікпен анықталады?
§37 Клаузиус теңсіздігі. Энтропия
1. Жүйеде өтетін дөңгелек процесс квазистатикалық болсын. Клаузиус теңсіздігі осындай процесті де сипаттайды:
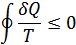
Тек бұл жағдайда Т қоршаған ортаның емес жүйенің температурасы, себебі бұл екі температура бірдей мәнге ие болады. Квазистатикалық процесс тек тар мағынада қайтымды болады. Демек, мұндай процесс кері бағытта да жүреді. Кері процесс үшін де Клаузиус теңсіздігі орындалады:
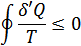
мұндағы 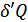 -кері процесте аз аралықтарда жүйе алатын элементар жылу мөлшерлері. Бұл жағдайда жүйе тура сол тепе-тең күйлерден кері бағытта өтетін болғандықтан
-кері процесте аз аралықтарда жүйе алатын элементар жылу мөлшерлері. Бұл жағдайда жүйе тура сол тепе-тең күйлерден кері бағытта өтетін болғандықтан 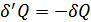 болады, сондықтан
болады, сондықтан 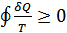 болады. Бұл қатынас алғашқы қатынаспен тек теңдік белгісі қойылғанда сәйкес болады. Осылай квазистатикалық процесс үшін Клаузиус теңсіздігі теңдікке айналады:
болады. Бұл қатынас алғашқы қатынаспен тек теңдік белгісі қойылғанда сәйкес болады. Осылай квазистатикалық процесс үшін Клаузиус теңсіздігі теңдікке айналады:
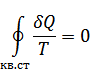
Термодинамиканың іргелі ұғымдарының бірі – энтропияның енгізілуі осы теңдікке негізделген.Термодинамиканың бірінші бастамасының жалпы тұжырымдамасын 1860 жылы Клаузиус енгізген және оны энтропия деп аталатын физикалық шаманы қолданып беруге болады.
| 30-сурет. |
| P |
| V |
| 1 |
| 0 |
| 2N |
| b |
| a |
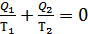 .
.
Енді кез келген қайтымды циклді қарастырайық (30-сурет). Кез келген қайтымды циклді жуықтап Карно циклдерінің тізбегі түрінде өрнектеуге болады. 30-суретте 12 қайтымды циклі 5Карно циклдерінің тізбегі түрінде көрсетілген, олардың әрқайсысы басқаларымен адиабаталық түрде байланысқан изотермалардан тұрады. Карно циклдерінің саны неғұрлым көп болса, олардың жуықтау дәрежесі соғұрлым жоғары болады.
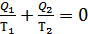 қатынасы осы циклдердің әрбіреуі үшін орындалады, сондықтан барлық циклдер үшін мына өрнек орындалады:
қатынасы осы циклдердің әрбіреуі үшін орындалады, сондықтан барлық циклдер үшін мына өрнек орындалады:
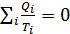 (37.1)
(37.1)
Мұндай қайтымды циклде әрбір цикл кезінде берілетін «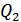 » жылу мөлшері, келесі циклде жүйе алатын «
» жылу мөлшері, келесі циклде жүйе алатын «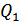 » жылу мөлшеріне тең болады. Сондықтан
» жылу мөлшеріне тең болады. Сондықтан 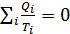 қатынасын Карно циклдерінің шексіз санынан тұратын кез келген қайтымды циклге қолдануға болады.
қатынасын Карно циклдерінің шексіз санынан тұратын кез келген қайтымды циклге қолдануға болады.
3. Жүйе бастапқы 1 -күйден соңғы 2 -күйге бірнеше квазистационар процестер болатын жолдармен өте алсын. Солардың екеуін қарастырайық – a және b жолдары. Осы процестерді бір 1a2b1 дөңгелек квазистатикалық процеске біріктіруге болады. Осы біріктірілген процеске Клаузиус теңдігін қолданайық:
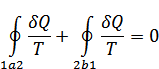
немесе
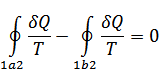
және
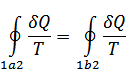
Жүйенің алған жылу мөлшерінің, сол жылу берілу кезіндегі абсолют температураға қатынасы келтірілген жылу мөлшері деп аталады. 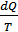 жүйенің өте аз процесс кезінде алған келтірілген жылу мөлшері болып табылады, ал
жүйенің өте аз процесс кезінде алған келтірілген жылу мөлшері болып табылады, ал 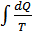 -интегралы процесс соңында жүйенің алған келтірілген жылу мөлшері. Келтірілген жылу мөлшері ұғымын қолданып Клаузиус теңдігін былай тұжырымдауға болады: «Кез келген квазистатикалық дөңгелек процесс кезіндегі жүйенің алған келтірілген жылу мөлшері нөлге тең» немесе осыған ұқсас «Жүйенің квазистатикалық алған келтірілген жылу мөлшері өту жолына тәуелсіз, тек жүйенің бастапқы және соңғы күйлерімен анықталады». Демек, келтірілген жылу мөлшері жүйенің күйлерін сипаттайды. Осының нәтижесінде жүйенің күйін сипаттайтын энтропия деп аталатын жаңа функцияны енгізуге болады.
-интегралы процесс соңында жүйенің алған келтірілген жылу мөлшері. Келтірілген жылу мөлшері ұғымын қолданып Клаузиус теңдігін былай тұжырымдауға болады: «Кез келген квазистатикалық дөңгелек процесс кезіндегі жүйенің алған келтірілген жылу мөлшері нөлге тең» немесе осыған ұқсас «Жүйенің квазистатикалық алған келтірілген жылу мөлшері өту жолына тәуелсіз, тек жүйенің бастапқы және соңғы күйлерімен анықталады». Демек, келтірілген жылу мөлшері жүйенің күйлерін сипаттайды. Осының нәтижесінде жүйенің күйін сипаттайтын энтропия деп аталатын жаңа функцияны енгізуге болады.
Энтропия – қандай да бір тұрақтыға дейінгі дәлдікпен анықталатын жүйенің күй функциясы. Тепе-тең 2- және 1- күйлеріндегі жүйе энтропиясының айырымы жүйені 1 -күйден 2 -күйге кез келген квазистатикалық жолмен өткізу үшін қажет келтірілген жылу мөлшеріне тең. Сонымен, энтропия күй параметрі болып табылады. Оның мәні тек жүйенің күйіне тәуелді, жүйенің осы күйге қандай процеспен және қалай келгеніне, жүйенің бұрынғы күйлеріне тәуелсіз.Егер 1, 2 күйлердегі энтропияны 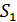 және
және 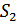 деп белгілесек, онда анықтамаға сәйкес:
деп белгілесек, онда анықтамаға сәйкес:

Энтропия дәлдігін анықтайтын қандайда бір тұрақтының мәні маңызды емес. Себебі, энтропияның өзінен гөрі оның айырмасы физикалық мағынаға ие. Шартты түрде қандай да бір күйдің энтропиясын нөлге тең деп алып тұрақтының мәнін анықтауға болады.
4. Сонымен, энтропия анықтамасы бойынша
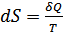 (37.3)
(37.3)
Осы қатынасты қолданып термодинамиканың бірінші бастамасын энтропия арқылы өрнектейік:
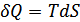 (37.4)
(37.4)
Ал термодинамиканың 1-бастамасына сәйкес
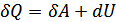
Егер жүйенің алған 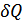 жылу мөлшерін(37.4)-өрнегіне сәйкес алмастырсақ, онда термодинамиканың 1-бастамасын мына түрде жаза аламыз:
жылу мөлшерін(37.4)-өрнегіне сәйкес алмастырсақ, онда термодинамиканың 1-бастамасын мына түрде жаза аламыз:
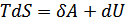 . (37.5)
. (37.5)
Егер жүйе өтетін айналмалы процесс қайтымсыз болса, онда 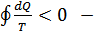 Клаузиус теңсіздігі орындалады. Демек,
Клаузиус теңсіздігі орындалады. Демек, 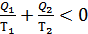 , ал энтропия өзгерісі қайтымсыз процесс кезінде былай анықталады
, ал энтропия өзгерісі қайтымсыз процесс кезінде былай анықталады 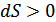 .
.
5. Мысал ретінде 1 моль идеал газдың энтропиясын анықтайық. Идеал газдағы кез келген өте аз квазистатикалық процесс үшін:
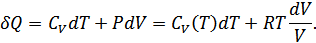
Осыдан
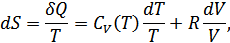
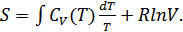 (37.6)
(37.6)
Егер 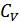 жылусиымдылығы тәуелді болмаса, онда интеграл оңай алынады:
жылусиымдылығы тәуелді болмаса, онда интеграл оңай алынады:
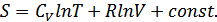 (37.7)
(37.7)
Егер газдың 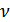 моль мөлшері берілген болса, онда
моль мөлшері берілген болса, онда
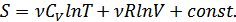 (37.8)
(37.8)
Бұл өрнек газдағы молекулалар саны өзгермейтін жағдай үшін алынды. Сондықтан теңдеудегі аддитивті тұрақты да газдағы бөлшектер санына тәуелді болады. Бұл тұрақтыны энтропия газдағы бөлшектер санына немесе мольдер санына пропорционал болатындай анықтау қажет. Бұл шартты мына өрнек қанағаттандырады:
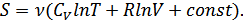
§38. Энтропияның өсу заңы
1. Жүйе тепе тең 1-күйден 2-тепе тең күйге өтсін (31-сурет), бірақ өту процесі қайтымсыз болсын (суретте қайтымсыз процесс штрих сызықпен I көрсетілген). Жүйені 2-күйден бастапқы 1-күйге квазистатикалық қандай да бір жолмен II қайтарайық. Клаузиустың теңсіздігі негізінде былай жазуға болады:
| 31-сурет |
| I |
| II |
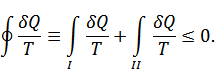
II процесі квазистатикалық болғандықтан
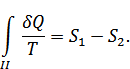
Сондықтан Клаузиус теңсіздігі мына түрге келеді:

Мұнда 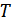 қоршаған ортаның температурасы. Осы температура кезінде ортадан жүйеге
қоршаған ортаның температурасы. Осы температура кезінде ортадан жүйеге 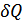 жылу мөлшері беріледі.
жылу мөлшері беріледі.
Егер жүйе адиабаталық оқшауланған болса, онда 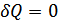 , және (38.1) интегралы нөлге тең болады. Онда
, және (38.1) интегралы нөлге тең болады. Онда
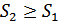 (38.2)
(38.2)
Адиабаталық оқшауланған жүйенің энтропиясы азаймайды, энтропия өсуі мүмкін немесе тұрақты болып қалуы керек. Бұл – энтропияның өсу заңы. Егер 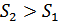 болса, онда адиабаттық оқшауланған жүйенің 2-күйден 1-күйге өтуі мүмкін емес, себебі бұл өту энтропияның кемуімен жүрер еді. Керісінше, жүйенің энтропиясы аз 1-күйден энтропиясы жоғары 2-күйге адиабатты өтуі термодинамиканың 2-бастамасының постулатына қайшы келмейді, демек, мүмкін. Осылай термодинамиканың 2-бастамасы табиғатта болатын процестің өту бағытын айқын көрсетеді.
болса, онда адиабаттық оқшауланған жүйенің 2-күйден 1-күйге өтуі мүмкін емес, себебі бұл өту энтропияның кемуімен жүрер еді. Керісінше, жүйенің энтропиясы аз 1-күйден энтропиясы жоғары 2-күйге адиабатты өтуі термодинамиканың 2-бастамасының постулатына қайшы келмейді, демек, мүмкін. Осылай термодинамиканың 2-бастамасы табиғатта болатын процестің өту бағытын айқын көрсетеді.
| Вакуум |
| V1 Газ |
| А |
| В |
| 30-сурет |
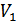 болатын бөлігінде болсын, ал ыдыстың екінші жағында вакуум болсын. Содан кейін АВ қабырғасы алып тасталсын немесе ол қабырғада тесік жасалсын. Газ ыдыстың екінші жағына аға бастайды. Ыдыстың екі жағындағы қысым мен температура теңескен соң бұл процесс тоқтайды. Осы процестің қайтымды немесе қайтымсыз екендігін анықтайық. Ол үшін энтропияның өзгерісін есептеу керек. Бұл процесс кезінде газдың ішкі энергиясы өзгермеуі керек, себебі газ қатты адиабаттық қоршауда. Джоуль заңына сай газдың температурасы да өзгермеуі керек, себебі температура газдың ішкі энергиясымен бірмәнді анықталады. Процестің басындағы және аяғындағы температура мәндерін Т деп, ал
болатын бөлігінде болсын, ал ыдыстың екінші жағында вакуум болсын. Содан кейін АВ қабырғасы алып тасталсын немесе ол қабырғада тесік жасалсын. Газ ыдыстың екінші жағына аға бастайды. Ыдыстың екі жағындағы қысым мен температура теңескен соң бұл процесс тоқтайды. Осы процестің қайтымды немесе қайтымсыз екендігін анықтайық. Ол үшін энтропияның өзгерісін есептеу керек. Бұл процесс кезінде газдың ішкі энергиясы өзгермеуі керек, себебі газ қатты адиабаттық қоршауда. Джоуль заңына сай газдың температурасы да өзгермеуі керек, себебі температура газдың ішкі энергиясымен бірмәнді анықталады. Процестің басындағы және аяғындағы температура мәндерін Т деп, ал 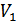 -бастапқы,
-бастапқы, 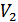 -соңғы көлемдерді белгілейік. Газдың энтропиясының өзгерісін есептеу үшін газды бастапқы күйден соңғы күйге квазистатикалық көшіру керек. Ол үшін газды температурасы Т қыздырғышпен жылулық жанастырамыз. Газға түсірілетін қысымды шексіз аз азайта отырып оны изотермиялық көлемі
-соңғы көлемдерді белгілейік. Газдың энтропиясының өзгерісін есептеу үшін газды бастапқы күйден соңғы күйге квазистатикалық көшіру керек. Ол үшін газды температурасы Т қыздырғышпен жылулық жанастырамыз. Газға түсірілетін қысымды шексіз аз азайта отырып оны изотермиялық көлемі 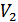 болатын соңғы күйге көшіреміз. Бұл кезде газ қыздырғыштан жылу мөлшерін алып оны эквивалентті жұмысқа айналдырады.
болатын соңғы күйге көшіреміз. Бұл кезде газ қыздырғыштан жылу мөлшерін алып оны эквивалентті жұмысқа айналдырады. Изотермиялық процесс үшін
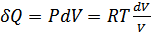 ,
,
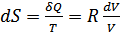 .
.
Осыдан энтропия өзгерісін былай анықтаймыз:
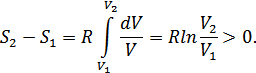
Демек, энтропия өсті. Сондықтан газдың бос кеңістікке адиабаталық ұлғаюы қайтымсыз процесс.
§39. Газдардың диффузиясы кезінде энтропияның өсуі.
 2015-04-30
2015-04-30 5744
5744








