Абсорбцией называют процесс избирательного поглощения компонентов из газовых или парогазовых смесей, как правило, жидкими поглотителями (абсорбентами). В отличие от адсорбции компоненты поглощаются во всем объеме абсорбента.
Различают физическую и химическую абсорбцию (хемосорбцию). При физической абсорбции поглощаемый компонент не вступает в химическую реакцию с абсорбентом. Процесс абсорбции в большинстве случаев обратим. На этом свойстве основан обратный процесс выделения поглощенного компонента из раствора - десорбция. При хемосорбции поглощаемый компонент образует с абсорбентом химическое соединение. В промышленности процесс абсорбции обычно сочетают с десорбцией, что позволяет многократно использовать абсорбент.
Примерами использования абсорбции в химическом производстве могут служить процессы разделения газообразных углеводородов на нефтеперерабатывающих установках, получение со-
ляной и серной кислот, аммиачной воды, очистка газовых выбросов от вредных примесей, выделение ценных компонентов из продуктов крекинга или пиролиза метана, из газов коксовых печей и т.д. Процесс абсорбции часто сопровождается выделением теплоты.
Жидкие поглотители (абсорбенты) выбирают по степени растворимости в них поглощаемых компонентов. Степень растворимости газов в жидких поглотителях зависит от физических и химических свойств газовой и жидкой фаз, температуры и давления газа в смеси.
Очевидно, что с практической точки зрения лучшим из ряда возможных будет тот поглотитель, расход которого при проведении данного процесса окажется наименьшим.
Для абсорбционно-десорбционных процессов равновесие между газами и их растворами описывается законом Генри, согласно которому при данной температуре количество газа, растворяющегося в жидкости, прямо пропорционально парциальному давлению газа над ней:
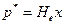 , (18.1)
, (18.1)
где 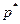 — равновесное парциальное давление растворяемого газа, Па; х — мольная доля растворенного компонента в жидкости;
— равновесное парциальное давление растворяемого газа, Па; х — мольная доля растворенного компонента в жидкости; 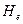 — константа Генри, Па, зависящая от свойств растворенного газа и поглотителя, а также температуры.
— константа Генри, Па, зависящая от свойств растворенного газа и поглотителя, а также температуры.
Под парциальным давлением газа понимают такое давление, которое создавал бы газ, если бы из газовой смеси были удалены все остальные компоненты при условии, что температура и объем системы сохранились неизменными.
Закон Генри применим для слаборастворимых газов, а также хорошо растворимых газов низкой концентрации.
Растворимость многих газов значительно отклоняется от закона Генри, и при расчетах рекомендуется пользоваться полученными из опыта значениями равновесного парциального давления 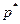 для соответствующих значений х.
для соответствующих значений х.
Согласно закону Дальтона парциальное давление компонента в газовой смеси пропорционально общему давлению:
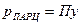 , (18.2)
, (18.2)
где у — мольная доля абсорбируемого компонента в газовой смеси; 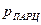 — парциальное давление газа; П — общее давление газовой смеси.
— парциальное давление газа; П — общее давление газовой смеси.
Таким образом, совместное решение уравнений (18.1) и (18.2) позволяет записать для равновесного состояния:
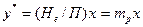 , (18.3)
, (18.3)
где 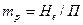 ;
; 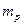 — коэффициент распределения, постоянный для данной системы газ—жидкость (при Т = const и П = const).
— коэффициент распределения, постоянный для данной системы газ—жидкость (при Т = const и П = const).
равнение (18.3) описывает прямую линию с тангенсом угла наклона, равным 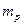 , и называется уравнением равновесия для процесса абсорбции при низких концентрациях растворов газов.
, и называется уравнением равновесия для процесса абсорбции при низких концентрациях растворов газов.
Из закона Генри следует, что растворимость газа в жидкости увеличивается по мере повышения давления и понижения температуры.
Для понижения температуры жидкости исходные вещества охлаждают с помощью теплообменников.
 2015-05-05
2015-05-05 3070
3070
