Топливо - это вещество, которое при окислении выделяет большое количество тепловой энергии.
Газообразное топливо представляет собой смесь горючих и негорючих газов, содержащую некоторое количество примесей. К горючим газам относятся углеводороды, водород и оксид углерода (угарный газ). Негорючие компоненты - это азот, диоксид углерода (углекислый газ) и кислород. К примесям относят водяные пары, сероводород, пыль, нафталин, аммиак и др. Негорючие газы и примеси составляют балласт газообразного топлива.
К горючим компонентам газообразного топлива относятся следующие вещества:
Метан СН4 - бесцветный, нетоксичный газ без запаха и вкуса. В состав метана входит 25 % водорода и 75 % углерода (по массе). При атмосферном давлении и температуре 111 К метан сжижается и его объем уменьшается почти в 600 раз. Сжиженный метан является перспективным топливом для многих отраслей народного хозяйства. И концентрации метана в воздухе более 10 % вызывает удушье.
Кроме метана в горючих газах могут содержаться этан – С2Н6 пропан - С3Н8, бутан - С4Н10, пентан - С5Н12 - углеводороды метанового ряда, которые носят название алканов, то есть насыщенных углеводородов. Общая формула алканов – СnН2n+2- Свойства их аналогичны свойствам метана. Пропан, бутан и пентан тяжелее воздуха, при концентрации в воздухе более 10 % и при вдыхании более 2 мин начинается головокружение, а затем наступает удушье. С увеличением числа атомов в молекуле тяжёлых углеводородов возрастают их плотность и теплота сгорания.
|
|
|
Оксид углерода CO (угарный газ) - бесцветный газ, без запаха и вкуса. Оксид углерода оказывает на организм человека токсичное воздействие, так как легко вступает в соединение с гемоглобином крови. Влияние концентрации СО на организм человека показано в таблице 1. Вследствие малого объёма продуктов горения CO на каждый куб. метр их приходиться меньше чем на 1 куб. метр продуктов горения углеводородов. Поэтому продукты горения CO нагреваются до более высокой температуры (1 CO - образует 2,88 м3 продуктов сгорания).
Водород Н2 - бесцветный нетоксичный газ без вкуса и запаха. Водород отличается высокой реакционной способностью, водородно-воздушные смеси имеют широкие пределы воспламенения и весьма взрывоопасны.
В негорючую часть газообразного топлива входит азот и углекислый газ.
Азот N2 - бесцветный газ без запаха и вкуса. Азот практически не реагирует с кислородом, поэтому при расчётах процесса горения его рассматривают как инертный газ.
Таблица 1. Физиологическое воздействие оксида углерода CO на организм человека.
| Содержание СО | Длительность и характер воздействия | |
| об. % | мг / л | |
| 0,01 | 0,125 | В течение нескольких часов не оказывает воздействия |
| 0,05 | 0,625 | В течении 1 часа нет заметного воздействия |
| 0,1 | 1,25 | Через 1 час наблюдается головная боль, тошнота, недомогание |
| 0,5 | 6,25 | Через 20 - 30 мин. оказывает смертельное воздействие |
Углекислый газ СО2 - бесцветный газ, тяжелее воздуха. Имеет слегка кисловатый запах и вкус. Концентрация в воздухе в пределах 4-5% приводит к сильному раздражению органов дыхания; 10% - ная концентрация СО2 в воздухе вызывает сильное отравление. При сильном охлаждении СО2 застывает в белую снегообразную массу. Твёрдый СО2 (сухой лёд) широко используется для хранения скоропортящихся продуктов.
|
|
|
Кислород О2 - без запаха, цвета и вкуса. Содержание кислорода в газе понижает теплоту сгорания и делает газ взрывоопасным. Поэтому содержание кислорода в газе не должно быть более 1% по объёму.
К вредным примесям относят сероводород.
Сероводород Н2 - газ с сильным и неприятным запахом, обладает высокой токсичностью. Сероводород является газообразной кислотой и, воздействуя на металлы, образует сульфиды. При сжигании газа Н2 сгорает и образует сернистый газ, вредный для здоровья. Содержание Н2 не должно превышать 2г на 100 м3 газа.
К основным характеристикам газообразного топлива относят: теплоту сгорания, плотность, число Воббе.
Теплотой сгорания топлива называется количество теплоты, которое выделяется при полном сгорании единицы топлива при постоянном давлении (Для газобразного топлива за единицу измерения принят 1 м3).
Различают низшую теплоту сгорания, Qн, и высшую - Qв.
Высшая теплота сгорания газового топлива соответствует условию, при котором водяные пары продуктов сгорания доводятся до жидкого состояния. В реальных условиях сжигания газа водяные пары не конденсируются, а находятся в парообразном состоянии. Понятие высшей теплоты сгорания относится только к тем газам, которые при сгорании выделяют водяные пары. Разница между Qн и Qв составляет 2514 кДж на каждый кг водяных паров, т.е
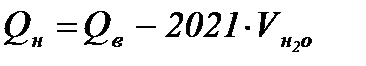 , кДж/м3,
, кДж/м3,
где 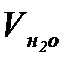 - объём водяных паров в продуктах сгорания при сжигании 1 м3 газа.
- объём водяных паров в продуктах сгорания при сжигании 1 м3 газа.
Почти все основные характеристики газового топлива могут быть определены, если известен его состав, по свойствам простых газов -компонентов смеси. Основные характеристики газов приведены в таблицах 2 и 3.
Теплоту сгорания смеси простых горючих газов подсчитывают по формуле
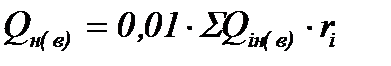 , кДж/м3,
, кДж/м3,
где ri - содержание горючих компонентов смеси, % по объему;
Qiн(в) - теплота сгорания каждого отдельного компонента, кДж/м3. (Принимается по таблице 3)
Таблица 2 Физические характеристики газов
| Газ | Химиче- ская формула | Молекулярная масса | Молеку- лярный объем прн 0°С 101,3 кПа, м3/кмоль | Плотность при О °С, 101,3 кПа, кг/ м3 | Относительная плотность по воздуху |
| Азот | N2 | 28.016 | 22,4 | 1.2505 | 0,9673 |
| Ацетилен | С3H3 | 26.038 | 22,24 1.1707 | 0,9055 | |
| Водород | Н2 | 2,016 | 22,43 | 0.08999 | 0,0695 |
| Водяной пар | Н2О | 18,016 | (23,45) | (0.768) | 0.5941 |
| Воздух (без СО2) | — | 28,96 | 22,4 | 1.2928 | |
| Диоксид серы | 502 | 64,066 | 21.89 | 2,9263 | 2,2635 |
| Диоксид углерода | СО2 | 44,011 | 22.26 | 1,9768 | 1,5291 |
| Кислород | О2 | 22,39 | 1,429 | 1,1053 | |
| Оксид углерода | СО | 28,011 | 22.41 | 1,25 | 0,9669 |
| Сероводород | Н25 | 34,082 | 22,14 | 1,5392 | 1,1906 |
| Метан | СН4 | 16,043 | 22,38 | 0,7168 | 0,5545 |
| Этан | С2Н6 | 30,07 | 22,18 | 1.3566 | 1,049 |
| Пропан | С3Н8 | 44,097 | 21.84 | 2.019 | 1,562 |
| Н-бутан | С4Н10 | 58,124 | 21,5 | 2,703 | 2,09] |
| Изобутан | С4Н10 | 58,124 | 21.78 | 2,668 | 2,064 |
| Пентан | С5Н12 | 72.151 | — | 3,221 | 2,491 |
Плотность газообразного топлива при температуре 0 0С и давлении 101,3 кПа определяется по формуле
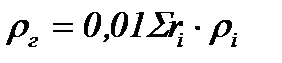 , кг/м3,
, кг/м3,
где ri - плотность отдельной компоненты газообразного топлива при температуре 0 0С и давлении 101,3 кПа, кг/м3 (принимаются по таблице 2);
ri - содержание отдельной компоненты газообразного топлива, % по объему.
Относительная плотность газа по воздуху определяется по формуле
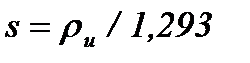
Таблица 3 Теплота сгорания чистых горючих газов
| Теплота сгорания | ||||||
| Газ | высшая | низшая | высшая | низшая | высшая | низшая |
| кДж/кмоль | кДж/кг | кДж/м3 при 0 0 С и 101,3 кПа | ||||
| Ацетилен | ||||||
| Водород | ||||||
| Оксид углерода | ||||||
| Сероводород | ||||||
| Метан | ||||||
| Этан | ||||||
| Пропан | ||||||
| Н-Бутан | ||||||
| Изобутан | ||||||
| Пентан |
Число Воббе, представляет собой отношение теплоты сгорания к корню квадратному из относительной плотности газа по воздуху.
|
|
|
Число Воббе (низшее или высшее) определяют по формулам, кДж/м3
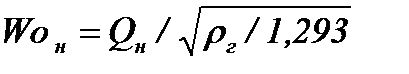 , кДж/м3,
, кДж/м3,
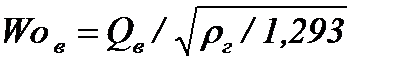 , кДж/м3,
, кДж/м3,
где Qн и Qв - низшая и высшая теплота сгорания газового топлива, кДж/м3;
rг - плотность газа при нормальных условиях, кг/м3.
Если газовое топливо является влажным, то производят пересчет теплоты сгорания и плотности топлива, которые были определены по сухому составу, по следующим формулам пересчета
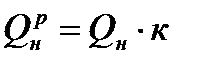 , кДж/м3,
, кДж/м3,
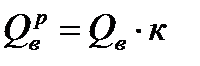 . кДж/м3,
. кДж/м3,
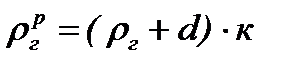 , кг/м3,
, кг/м3,
где к - коэффициент пересчета, определяемый по формуле
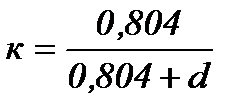 ,
,
где d - влагосодержание газа, выраженное в кг на I м3 сухого газа при температуре 0°С и давлении 101,3 кПа.
Принадлежность всех углеводородов, составляющих горючую часть газового топлива, к одному гомологическому ряду позволяет упростить ряд важнейших зависимостей, выражающих теплофизические свойства природного газа, и определить их, не зная содержания отдельных компонентов в нем. Это возможно благодаря тому, что углеводороды метанового ряда (алканы) имеют общую формулу CnH2n+2n, где n - так называемое углеродное число.
Углеродное число сравнительно просто может быть определено с помощью газоанализатора с дожиганием или же подсчитано по известному объемному составу природного газа по формуле
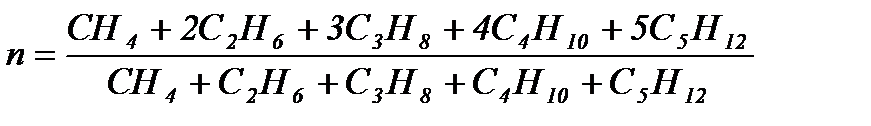 ,
,
где CH4, C2H6 и т.д. - содержание углеводородов в сухом газе, %.
Величина n всегда больше единицы и может быть дробной.
Основные характеристики сухого природного газа могут быть подсчитаны по следующим формулам:
высшая теплота сгорания, кДж/м3
Qв=(295,3n + 102,6)r,
низшая теплота сгорания, кДж/м3
Qн= (276,5 n + 81,7)r,
плотность (в нормальных условиях), кг/м3
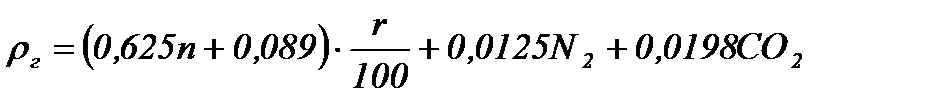 ,
,
газовая постоянная, Дж/(кг К)
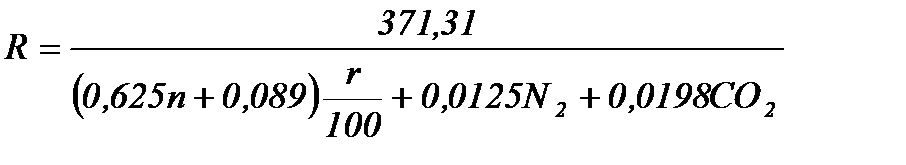 ,
,
кажущаяся молекулярная масса
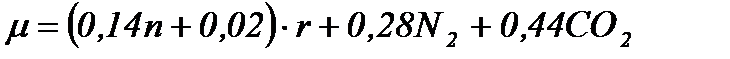 ,
,
Объемная теплоемкость при постоянном давлении (для диапазона температур 0 - 50°С), кДж/(м8 К)
|
|
|
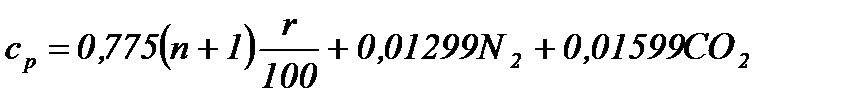 ,
,
покаэатель адиабаты
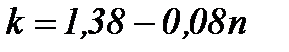 ,
,
кинематическая вязкость, м2/с
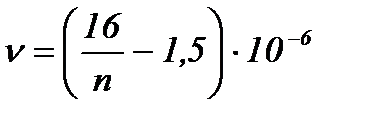 ,
,
Объём газа измеряется в м3. В связи с тем, что объём газов значительно изменяется при нагревании, охлаждении и сжатии для сравнения количеств газа их приводят к нормальным и стандартным условиям.
Нормальные условия: температура 0 оС и давление 101325 Па (760 мм рт ст). Объем газа при данных условиях может быть определен по формуле
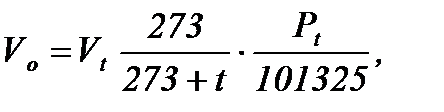 м3/ч.
м3/ч.
Стандартные условия: температура 20 0С и давление 101325 Па. Объем газа при данных условиях может быть определен по формуле
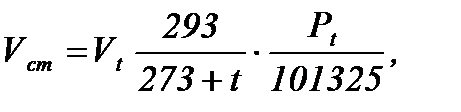 м3/ч.
м3/ч.
где Pt - абсолютное давление газа в момент изменения, Па.
t - температура газа,.
Vt - объём газа при заданном давлении Pt и температуре t.
При изменении расхода газа по расходомерам.
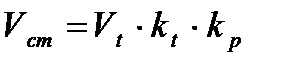 , м3/ч,
, м3/ч,
где 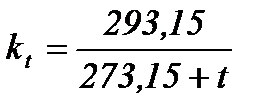 іи
іи 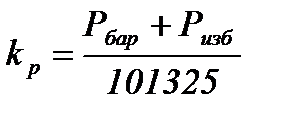
Для влажного газа.
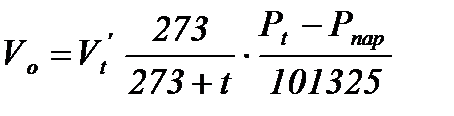 , м3/ч;
, м3/ч;
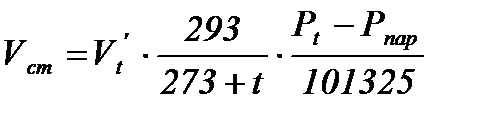 , м3/ч,
, м3/ч,
где Pпар - упругость водяных паров, Па, при температуре t, 0С.
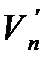 - объём влажного газа, м3/ч.
- объём влажного газа, м3/ч.
Нормальные условия используются при гидравлических расчётах газопроводов, стандартные - при расчётах за газ.
 2015-04-20
2015-04-20 18681
18681
