Все примеси, загрязняющие природную воду, можно разделить по степени дисперсности (крупности):
1) Грубодисперсные с размерами частиц более 100 нм;
2) Коллоиднодисперсные с размерами частиц от 1 до 100 нм;
3) Молекулярнодисперсные с размерами частиц менее 1 нм.
Грубодисперсные примеси обуславливают мутность природных вод и являются механическими примесями, состоящими из песка, глины и т.д.
Коллоиднодисперсные вещества не осаждаются даже в течение длительного времени. В природных водах в коллоиднодисперсном состоянии находятся соединения кремния, алюминия, железа, а также органические вещества, образующиеся в результате распада животных и растительных организмов.
К молекулярнодисперсным примесям относятся растворенные в воде соли, кислоты, щелочи и газы. Ионы кальция занимают в водах первое место по содержанию. Основным источником появления ионов кальция в природных водах являются известняки.
По химическому составу примеси природных вод можно разделить на два типа: 1. минеральные и 2. органические.
К минеральным примесям воды относятся растворенные в ней содержащиеся в атмосфере газы N2, O2, СО2‚ образующиеся в результате окислительных и биохимических процессов NНЗ, СН4‚ Н2S‚ а также газы, вносимые сточными водами; различные соли, кислоты, основания, в значительной степени находящиеся в диссоциированной форме, т.е. в виде образующих их катионов и анионов.
К органическим примесям природных вод относят гумусовые вещества, вымываемые из почв и торфяников, а также органические вещества различных типов, поступающие в воду совместно с сельскохозяйственными стоками и другими типами недостаточно очищенных стоков.
Высокоосновные аниониты. Зависимость обменной емкости от рН среды. Объяснить, как изменяются показатели качества воды после высокоосновного анионирования. Почему высокоосновные аниониты ставят в схемах водоочистки в ее последних ступенях?
Иониты представляют собой нерастворимые в воде вещества, которые благодаря наличию в них специальных функциональных групп способны к реакциям ионного обмена.
Высокое значение Рн в зоне обмена на анионите способствует диссоциации слабых кислот Н2СО3 и Н2SiO3 и переводу их в ионизированное состояние, поэтому они также могут участвовать в реакциях анионного обмена, но лишь при использовании сильноосновных анионитов:
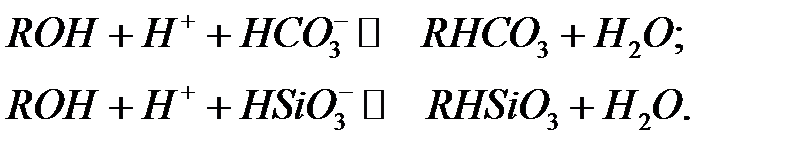
С учётом значений обменных емкостей слабоосновных и сильноосновных анионитов ( ), а так же способности только последних собирать аниониты слабых кислот схемы химического обессоливания обычно содержат две ступени анионирования: на первой ступени в фильтры загружается слабоосновный анионит, удаляющий ионы
), а так же способности только последних собирать аниониты слабых кислот схемы химического обессоливания обычно содержат две ступени анионирования: на первой ступени в фильтры загружается слабоосновный анионит, удаляющий ионы 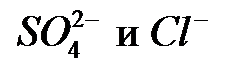 ; на второй ступени – сильноосновный (высокоосновный) анионит, предназначенный главным образом для обескремнивания воды.
; на второй ступени – сильноосновный (высокоосновный) анионит, предназначенный главным образом для обескремнивания воды.
 2015-05-14
2015-05-14 6596
6596
