1. Из записи химической формулы горения октана в кислороде в виде
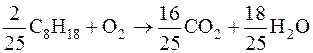
следует, что в одном киломоле молекулярного кислорода может полностью сгореть 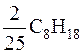 киломоля октана. С учетом молярных масс газов имеем: для полного сжигания
киломоля октана. С учетом молярных масс газов имеем: для полного сжигания 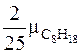 кг октана требуется
кг октана требуется 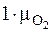 кг молекулярного кислорода. А так как в одном килограмме сухого воздуха содержится
кг молекулярного кислорода. А так как в одном килограмме сухого воздуха содержится 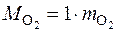 кг кислорода, то из пропорции
кг кислорода, то из пропорции
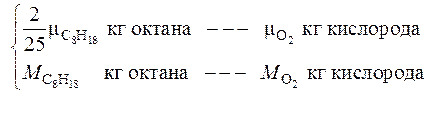
находим массу октана, которая может полностью сгореть в 1 кг сухого воздуха:
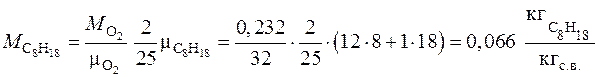
2. Вычислим физические свойства смеси «бензин–воздух» при нормальных физических условиях. Массовый состав смеси «октан–воздух»:
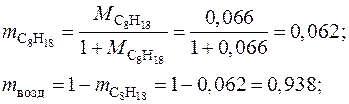
Объемный состав смеси:
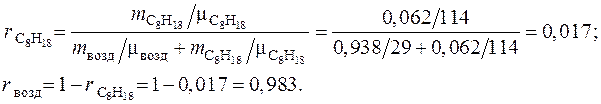
Молекулярная масса смеси:
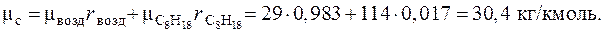
Газовая постоянная смеси:
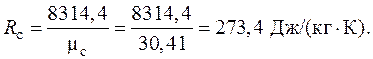
Плотность смеси при н.ф.у.:
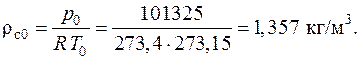
3. Вычислим физические свойства продуктов сгорания смеси при нормальных физических условиях.
Из химической формулы горения октана в кислороде составим пропорции, аналогично п.1:
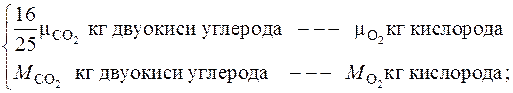
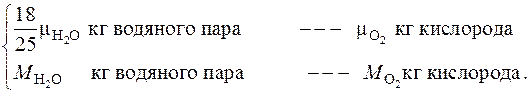
Отсюда находим массы двуокиси углерода и водяного пара, входящих в состав продуктов полного сгорания бензина в одном килограмме сухого воздуха:
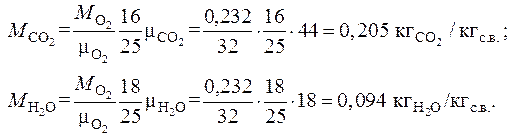
Продукты полного сгорания бензина в воздухе представляют собой смесь молекулярного азота, двуокиси углерода и водяного пара. В расчете на 1 кг сухого воздуха массы компонентов в продуктах сгорания будут следующими:
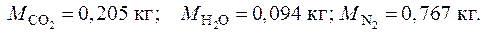
Зная массы компонентов и их молекулярные массы, стандартным методом находим массовый и объемный состав продуктов сгорания, их молекулярную массу, газовую постоянную и плотность при н.ф.у.:
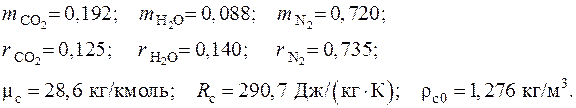
4. С целью сравнения вычисленных свойств смеси паров бензина с воздухом в стехиометрическом отношении и продуктов полного сгорания такой смеси со свойствами стандартного атмосферного сухого воздуха составим следующую таблицу, включающую известные свойства сухого воздуха и вычисленные свойства смехиометрической смеси паров бензина с воздухом и продуктов сгорания этой смеси:
| Смесь | 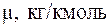 | 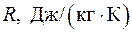 | 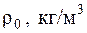 |
| Чистый воздух | 28,95 | 287,0 | 1,293 |
| Бензин+воздух | 30,41 | 273,4 | 1,357 |
| Продукты сгорания | 28,60 | 290,7 | 1,276 |
Из приведенной таблицы следует, что физические свойства стехиометрической смеси паров бензина с воздухом и продуктов сгорания незначительно отличаются от физических свойств чистого воздуха.
2.10. Газовая смесь, состоящая из углекислого газа, азота и кислорода, находится в резервуаре под давлением 5 бар при температуре 40 оС. Парциальные давления компонентов смеси равны: 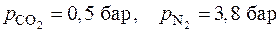 . Определить состав смеси в объемных и в массовых долях и плотность смеси.
. Определить состав смеси в объемных и в массовых долях и плотность смеси.
Ответ: 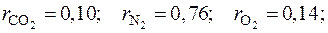
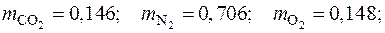
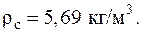
2.11. В баллоне емкостью 1 м3 находится воздух при давлении 2 бара и температуре 20 оС. Сколько надо накачать в баллон азота, чтобы давление в нем достигло 10 бар при той же температуре?
Ответ: 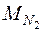 = 9,2 кг.
= 9,2 кг.
2.12. До какого давления по манометру надо довести смесь газов состава: 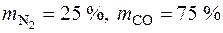 , чтобы парциальное давление азота в ней было 1,2 бар? Какое давление при этом будет иметь СО? Атмосферное давление p бар = 1,04 бар.
, чтобы парциальное давление азота в ней было 1,2 бар? Какое давление при этом будет иметь СО? Атмосферное давление p бар = 1,04 бар.
Ответ: 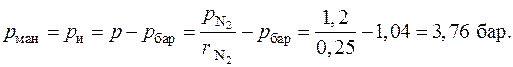
2.13. Смесь водорода H2 и метана CH4, занимающая объем V = 67,2 м3, имеет газовую постоянную R = 2550 Дж/(кг×К), давление p с = 0,98 бар и температуру t с = 15 оС. Определить массовый и объемный состав смеси, массы водорода и метана в смеси.
 2015-05-13
2015-05-13 2255
2255








