Избыточная энергия, которой должны обладать молекулы для того, чтобы их столкновение могло привести к образованию нового вещества, называется энергией активации данной реакции. Энергию активации выражают в кДж/моль. Молекулы, обладающие такой энергией, называются активными молекулами.
Возрастание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости реакции — числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10 градусов. Температурный коэффициент различных реакций различен. При обычных температурах его значение для большинства реакций лежит в пределах от 2 до 4.
Реакции, требующие для своего протекания заметной энергии активации, начинаются с разрыва или с ослабления связей между атомами в молекулах исходных веществ. При этом вещества переходят в неустойчивое промежуточное состояние, характеризующееся большим запасом энергии. Это состояние называется активированным комплексом. Именно для его образования и необходима энергия активации.
|
|
|
Если Еа<40 кДж/моль, то скорость очень велика, если Еа>120 кДж/моль, то скорость очень мала.
Температурное правило Вант-Гоффа: При увеличении температуры на каждые 10° скорость хм реакции взрастает в 2 – 4 раза; при уменьшении температуры – уменьшается во столько же раз.
u 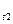 /u
/u 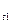 =g
=g 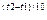 ; g=2..4. Для денатурации g»50.
; g=2..4. Для денатурации g»50.
Причина температурной зависимости обусловлено тем, что частицы при повышении температуры движутся быстрее и чаще сталкиваются.
 2015-05-30
2015-05-30 591
591








