При решении задач на эту тему рекомендуется:
– использовать уравнение Менделеева-Клапейрона, если состояние газа не меняется. Если при этом давление Р и объем газа V не заданы, то их следует выразить через величины, заданные в условии задачи;
– если в задаче рассматривается несколько состояний газа, то параметры этих состояний обозначают следующим образом: 1-е состояние – m 1, P 1, V 1, T 1; 2-е состояние – m 2, P 2, V 2, T 2 и т.д., а затем используют для каждого из состояний уравнение Менделеева-Клапейрона (если масса газа m изменяется) или уравнение Клапейрона 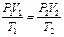 (если масса газа не изменяется);
(если масса газа не изменяется);
– если один из параметров газа остается постоянным и масса газа не меняется, то используют один из законов идеального газа: Бойля-Мариотта (T =const), Гей-Люссака (при Р =const) и Шарля (при V =const);
– при решении задач, в которых рассматриваются процессы, связанные с изменением состояний нескольких газов все выше названные действия следует проделать для каждого газа отдельно;
– решить полученные уравнения (дополненные в случае необходимости другими соотношениями, которые следуют из условия задачи) и найти искомые величины.
 2015-06-05
2015-06-05 331
331








