Могут ли в растворе существовать совместно следующие вещества: FeCl2 и KMnO4; NiCl2 и NaOH; FeCl2 и K4[Fe(CN)6]? Составьте уравнения реакций.
Решение.
Указанные пары могут существовать совместно, если между ними не будут протекать окислительно-восстановительные реакции или реакции обмена.
Степень окисления железа в FeCl2, равная (+2), – промежуточная, а марганца в KMnO4, равная (+7), – высшая. Следовательно, эти вещества будут взаимодействовать, причем KMnO4 – окислитель, а FeCl2 – восстановитель.
Напишем реакции:
3FeCl2 + KMnO4 + 2H2O = 3FeOHCl2 + MnO2 +KOH,
3Fe2+ + MnO 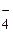 + 2H2O = 3Fe3+ + MnO2.
+ 2H2O = 3Fe3+ + MnO2.
Раствор хлорида никеля содержит только ионы Ni2+ и Cl–. Гидроксид натрия также полностью диссоциирует в растворе на ионы Na+ и OH–. При смешивании растворов NiCl2 и NaOH ионы Ni2+ и OH– связываются друг с другом и образуют нерастворимый в воде гидроксид никеля (II):
NiCl2 + 2NaOH = Ni(OH)2 + 2NaCl,
Ni2+ + 2OH– = Ni(OH)2¯.
В водном растворе FeCl2 и K4[Fe(CN)6] диссоциируют по уравнениям:
FeCl2 D Fe2+ + 2Cl–,
K4[Fe(CN)6] ® 4K+ + [Fe(CN)6]4–.
При смешивании растворов никакие комбинации ионов Fe2+, K+, Cl–, [Fe(CN)6]4– не приводят к образованию малорастворимого, летучего или слабо-диссоциирующего вещества. Следовательно, никакой реакции не происходит.
|
|
|
Итак, в растворе могут существовать совместно только FeCl2 и K4[Fe(CN)6].
 2015-06-24
2015-06-24 640
640








