(лат. ad — на, при; sorbeo — поглощаю) — увеличение концентрации растворенного вещества у поверхности раздела двух фаз (твердая фаза-жидкость, конденсированная фаза - газ) вследствие нескомпенсированности сил межмолекулярного взаимодействия на разделе фаз[1]. Адсорбция является частным случаем сорбции, процесс, обратный адсорбции - десорбция[2].
Содержание [убрать]
|
Основные понятия [править]
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция. Если скорости адсорбции и десорбции равны, то говорят об установлении адсорбционного равновесия. В состоянии равновесия количество адсорбированных молекул остается постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и состав системы)[3].
|
|
|
Адсорбция и хемосорбция [править]
На поверхности раздела двух фаз помимо адсорбции, обусловленной в основном физическими взаимодействиями (главным образом это Ван-дер-Ваальсовы силы), может идти химическая реакция. Этот процесс называется хемосорбцией. Чёткое разделение на адсорбцию и хемосорбцию не всегда возможно. Одним из основных параметров по которым различаются эти явления является тепловой эффект: так, тепловой эффект физической адсорбции обычно близок к теплоте сжижения адсорбата, тепловой эффект хемосорбции значительно выше. Кроме того в отличие от адсорбции хемосорбция обычно является необратимой и локализованной. Примером промежуточных вариантов, сочетающих черты и адсорбции и хемосорбции является взаимодействие кислорода на металлах и водорода на никеле: при низких температурах они адсорбируются по законам физической адсорбции, но при повышении температуры начинает протекать хемосорбция.
Схожие явления [править]
В предыдущем разделе говорилось о случае протекания гетерогенной реакции на поверхности- хемосорбции. Однако бывают случаи гетерогенных реакций по всему объему, а не только на поверхности- это обычная гетерогенная реакция. Поглощение по всему объёму может проходить и под воздействием физических сил- этот случай называется абсорбцией.
|
|
|
| Виды взаимодействий | Взаимодействия только на поверхности | Взаимодействия по всему объёму |
| Физические | Адсорбция | Абсорбция |
| Химические | Хемосорбция | Гетерогенная реакция |
Физическая адсорбция [править]
| Модели физической адсорбции | |
| Образование монослоя | Энергетическая диаграмма |
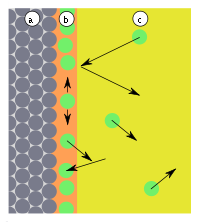 | 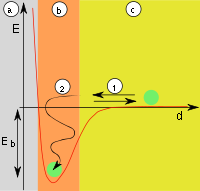 |
| Рис. 1: a) адсорбент, b) адсорбат, c) адсорбтив (газовая фаза или раствор) | Рис. 2: a) адсорбент, b) адсорбат, c) газовая фаза, d - расстояние, E - энергия, Eb - энергия адсорбции, (1) десорбция, (2) адсорбция |
| Поликонденсация | Избирательная адсорбция |
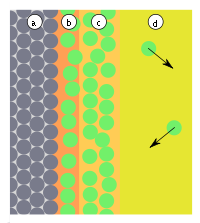 | 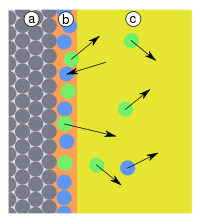 |
| Рис. 3: a) адсорбент, b) адсорбат, c) конденсат, d) адсорбтив (газовая фаза или раствор) | Рис. 4: a) адсорбент, b) адсорбат, c) адсорбтивы (газовая фаза или раствор): показана преимущественная адсорбция частиц голубого цвета |
Причиной адсорбции являются неспецифические (то есть не зависящие от природы вещества) Ван-дер-Ваальсовы силы. Адсорбция, осложнённая химическим взаимодействием между адсорбентом и адсорбатом, является особым случаем. Явления такого рода называют хемосорбцией и химической адсорбцией. «Обычную» адсорбцию в случае, когда требуется подчеркнуть природу сил взаимодействия, называют физической адсорбцией.
Физическая адсорбция является обратимым процессом, условие равновесия определяется равными скоростями адсорбции молекул адсорбтива P на вакантных местах поверхности адсорбента S* и десорбции — освобождения адсорбата из связанного состояния S − P:
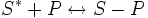 ;
;
уравнение равновесия в таком случае:
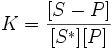 ,
,
где K — константа равновесия, [S − P] и [S*] — доли поверхности адсорбента, занятые и незанятые адсорбатом, а [P] — концентрация адсорбтива.
Количественно процесс физической мономолекулярной адсорбции в случае, когда межмолекулярным взаимодействием адсорбата можно пренебречь, описывается уравнением Ленгмюра:
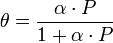 ,
,
где 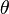 — доля площади поверхности адсорбента, занятая адсорбатом,
— доля площади поверхности адсорбента, занятая адсорбатом, 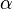 — адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива.
— адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива.
Поскольку 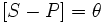 и, соответственно,
и, соответственно, 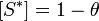 , уравнение адсорбционного равновесия может быть записано следующим образом:
, уравнение адсорбционного равновесия может быть записано следующим образом:
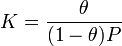
Уравнение Ленгмюра является одной из форм уравнения изотермы адсорбции. Под уравнением изотермы адсорбции (чаще применяют сокращённый термин — изотерма адсорбции) понимают зависимость равновесной величины адсорбции от концентрации адсорбтива a=f(С) при постоянной температуре (T=const). Концентрация адсорбтива для случая адсорбции из жидкости выражается, как правило, в мольных либо массовых долях. Часто, особенно в случае адсорбции из растворов, пользуются относительной величиной: С/Сs, где С — концентрация, Сs — предельная концентрация (концентрация насыщения) адсорбтива при данной температуре. В случае адсорбции из газовой фазы концентрация может быть выражена в единицах абсолютного давления, либо, что особенно типично для адсорбции паров, в относительных единицах: P/Ps, где P — давление пара, Ps — давление насыщенных паров этого вещества. Саму величину адсорбции можно выразить также в единицах концентрации (отношение числа молекул адсорбата к общему числу молекул на границе раздела фаз). Для адсорбции на твёрдых адсорбентах, особенно при рассмотрении практических задач, используют отношение массы или количества поглощённого вещества к массе адсорбента, например мг/г или ммоль/г.
Значение адсорбции [править]
Адсорбция — всеобщее и повсеместное явление, имеющее место всегда и везде, где есть поверхность раздела между фазами. Наибольшее практическое значение имеет адсорбцияповерхностно-активных веществ и адсорбция примесей из газа либо жидкости специальными высокоэффективными адсорбентами. В качестве адсорбентов могут выступать разнообразные материалы с высокой удельной поверхностью: пористый углерод (наиболее распространённая форма — активированный уголь), силикагели, цеолиты а также некоторые другие группы природных минералов и синтетических веществ.
|
|
|
Адсорбция (особенно хемосорбция) имеет также важное значение в гетерогенном катализе. Пример адсорбционных установок приведён на странице азотные установки.
Установка для проведения адсорбции называется адсорбером.
«Методы получения коллоидных растворов»
1. Какими признаками отличают коллоидные растворы от истинных?
Коллоидный раствор отличается от истинного раствора размерами частиц растворенного вещества: в истинных растворах размер частиц менее 10−9 м, частицы в таких растворах невозможно обнаружить оптическими методами; в то время как в коллоидных растворах размер частиц 10−9 м – 10−7 м.
2. Свойства коллоидных растворов.
По внешнему виду и некоторым свойствам коллоидные растворы похожи на обычные растворы солей и других, веществ. После фильтрации через плотную фильтровальную бумагу коллоидные растворы остаются прозрачными, не оставляют на ней осадка, их можно разбавлять водой или до известного предела сгущать без появления осадка и т. д.
Коллоидные растворы способны рассеивать свет (опалесцировать). Опалесценция становится особо заметной при рассматривании раствора в отраженном свете (явление Фарадея - Тиндаля). Коллоидные растворы в отличие от истинных очень медленно диффундируют. Отличаются они от истинных растворов и малой величиной осмотического давления.
Одним из отличий коллоидных растворов является их неустойчивость. Часто бывает достаточно прибавить к коллоидному раствору небольшое количество раствора электролита или нагреть его до определенной температуры, как начинает происходить укрупнение частиц дисперсной фазы (коагуляция), которые, достигнув известной величины, уже не могут удерживаться во взвешенном состоянии и выпадают в осадок (седиментация). Вообще, устойчивость коллоидных растворов зависит от ряда факторов: природы вещества дисперсной фазы, степени дисперсности и заряда частиц, вида дисперсионной среды и других. Степень влияния каждого из этих факторов на устойчивость коллоидного раствора неодинакова.
|
|
|
Характерной особенностью всех коллоидных растворов является и их самопроизвольное изменение во времени (старение), заканчивающееся самопроизвольной коагуляцией. Продолжительность процесса старения зависит от природы золя, его концентрации в растворе, способа изготовления и других условий. Для большинства золей процесс старения связан с уменьшением степени дисперсности коллоидных частиц.
3. В чем заключается сущность методов конденсации?
Эти методы также основаны на конденсационном выделении новой фазы из пересыщенного раствора. Однако в отличии от физических методов, вещество, образующее дисперсную фазу, появляется в результате химической реакции. Таким образом, любая химическая реакция, идущая с образованием новой фазы, может быть источником получения коллоидной системы. В качестве примеров приведем следующие химические процессы.
1.Восстановление. Классический пример этого метода – получение золя золота восстановлением золотохлористоводородной кислоты. В качестве восстановителя можно применять пероксид водорода (метод Зигмонди):
2HAuCl2+3H2O2®2Au+8HCl+3O2
Известны и другие восстановители: фосфор (М. Фарадей), таннин (В. Освальд), формальдегид (Р.Жигмонди). Например,
2KAuO2+3HCHO+K2CO3=2Au+3HCOOK+KHCO3+H2O
2.Окисление. Окислительные реакции широко распространены в природе. Это связано с тем, что при подъеме магматических расплавов и отделяющихся от них газов, флюидных фаз и подземных вод все подвижные фазы проходят из зоны восстановительных процессов на большой глубине к зонам окислительных реакций вблизи поверхности. Иллюстрацией такого рода процессов является образование золя серы в гидротермальных водах, с окислителями (сернистым газом или кислородом):
2H2S+O2=2S+2H2O
Другим примером может служить процесс окисления и гидролиза гидрокарбоната железа:
4Fe(HCO3)2+O2+2H2O®4Fe(OH)3+8CO2
Получающийся золь гидроокиси железа сообщает красно-коричневую окраску природным водам и является источником ржаво-бурых зон отложений в нижних слоях почвы.
3. Гидролиз. Широкое распространение в природе и важное значение в технике имеет образование гидрозолей в процессах гидролиза солей. Процессы гидролиза солей применяют для очистки сточных вод (гидроксид алюминия, получаемый гидролизом сульфата алюминия). Высокая удельная поверхность образующихся при гидролизе коллоидных гидроксидов позволяет эффективно адсорбировать примеси – молекулы ПАВ и ионы тяжелых металлов.
4. Реакции обмена. Этот метод наиболее часто встречается на практике. Например, получение золя сульфида мышьяка:
2H3AsO3+3H2S®As2S3+6H2O,
получение золя йодида серебра:
AgNO3+KI®AgI+KNO3
Интересно, что реакции обмена дают возможность получать золи в органических растворителях. В частности, хорошо изучена реакция
Hg(CN)2+H2S®HgS+2HCN
Ее проводят, растворяя Hg(CN)2 в метиловом, этиловом или пропиловом спирте и пропуская через раствор сероводород.
Хорошо известные в аналитической химии реакции, как, например, получение осадков сульфата бария или хлорида серебра
Na2SO4 + BaCl2® BaSO4 + 2NaCl
AgNO3 + NaCl ® AgCl + NaNO3
в определенных условиях приводят к получению почти прозрачных, слегка мутноватых золей, из которых в дальнейшем могут выпадать осадки.
Таким образом, для конденсационного получения золей необходимо, чтобы концентрация вещества в растворе превышала растворимость, т.е. раствор должен быть пересыщенным. Эти условия являются общими как для образования высокодисперсного золя, так и обычного осадка твердой фазы. Однако, в первом случае требуется соблюдение особых условий, которые, согласно теории, разработанной Веймарном, заключается в одновременности возникновения огромного числа зародышей дисперсной фазы. Под зародышем следует понимать минимальное скопление новой фазы, находящееся в равновесии с окружающей средой. Для получения высокодисперсной системы необходимо, чтобы скорость образования зародышей была намного больше, чем скорость роста кристаллов. Практически это достигается путем вливания концентрированного раствора одного компонента в очень разбавленный раствор другого при сильном перемешивании.
Золи образуются легче, если в процессе их получения в растворы вводят специальные соединения, называемые защитными веществами, или стабилизаторами. В качестве защитных веществ при получении гидрозолей применяют мыла, белки и другие соединения. Стабилизаторы используют и при получении органозолей.
4. В чём сущность пептизации?
Пептизация — расщепление агрегатов, возникших при коагуляции дисперсных систем, на первичные частицы под действием жидкой среды (например, воды) или специальных веществ — пептизаторов. Другими словами – это процесс обратный процессу коагуляции. Пептизация — один из способов получения коллоидных растворов, применяется в технике при получении высокодисперсных суспензий глин и других веществ.
5. Написать уравнение реакции и мицеллу получение золя берлинской лазури.
K4[Fe(CN)6]+2CuSO4=Cu2(Fe(CN)6)+2K2SO4
Мицеллярная формулу при избытке ионов Fe(CN)6 и FeCl3:
{m[Fe4[Fe(CN)6]3]∙n[Fe(CN)6]4-∙(4n-x)K+}x-∙xK+
{m[Fe4[Fe(CN)6]3]∙n[Fe]3+∙(n-x)Cl-}x+∙xCl-
Строение мицеллы гидрофобного золя. Коагуляция гидрофобного золя
Синтез гидрофобных дисперсных систем (суспензий, золей, в том числе аэрозолей, эмульсий) осуществляют методами диспергирования и конденсации. Диспергирование твердых и жидких веществ в выбранных средах проводят в шаровых и коллоидных мельницах вибропомола, ультразвуковых установках и др. Эффект усиливается при введение в среду ПАВ (эффект Ребиндера). Конденсационные методы основаны на физической или химической конденсации атомов или молекул с последующим образованием новой фазы в виде дисперсных частиц, распределенных в объёме среды (газообразной, жидкой или твердой).
Методом физической конденсации получают золи, дымы, дисперсные металлы. При химической конденсации частицы новой фазы образуются в результате протекания в системе химической реакции с образованием малорастворимых соединений.
Гидрофобные дисперсные системы термодинамически неустойчивы, так как частицы дисперсной фазы склонны к агрегации. Их термодинамическая агрегативная неустойчивость обусловлена избытком поверхностной энергии. Межфазное поверхностное натяжение в гидрофобных системах больше рассчитанного по соотношению Ребиндера-Щукина. Поэтому они не могут быть получены самопроизвольным диспергированием как лиофильныесистемы; для их образования должна быть затрачена внешняя энергия.
Укрупнение частиц дисперсной фазы при потере агрегативной устойчивости достигается в результате изотермической перегонки (растворение мелких и рост крупных частиц в соответствии с уравнением Кельвина) или за счет слипания (слияния) частиц – коагуляции. Наиболее распространен процесс коагуляции. В зависимости от природы системы и концентрации дисперсной фазы этот процесс может заканчиваться или осаждением частиц, или структурообразованием.
Гидрофобные дисперсные системы характеризуются кинетической агрегативной устойчивостью, определяемой скоростью процесса коагуляции. Кинетика коагуляции определяется уравнением Смолуховского:
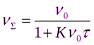 или
или 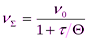
где 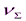 - суммарное число частиц дисперсной фазы ко времени τ;
- суммарное число частиц дисперсной фазы ко времени τ;  - первоначальное число частиц;
- первоначальное число частиц; 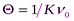 - время половинной коагуляции; ^ К – константа скорости коагуляции.
- время половинной коагуляции; ^ К – константа скорости коагуляции.
Константа К определяется соотношением
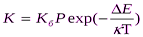 или
или 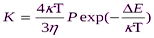
где Кб – константа скорости быстрой коагуляции; Р – стерический множитель, учитывающий благоприятные пространственные расположения частиц при столкновении; ΔЕ – энергия взаимодействия частиц, или потенциальный барьер; κ - константа Больцмана; η – вязкость дисперсионной среды.
Константа скорости коагуляции ^ К (константа скорости медленной коагуляции) является мерой кинетической агрегативной устойчивости. Если ΔЕ=0 и Р= 1, то эта константа равна константе скорости быстрой коагуляции, зависящей от вязкости среды и температуры системы. Если ΔЕ≠0 и Р≠1, то не все соударения частиц эффективны, и происходит медленная коагуляция. Замедление коагуляции, обусловленное потенциальным барьером, характеризуется фактором устойчивости, или коэффициентом стабильности:
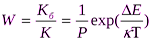
При значительном потенциальном барьере может наступить такое состояние системы, когда скорость агрегации частиц равна скорости дезагрегации и система окажется термодинамически устойчивой к коагуляции.
Таким образом, агрегативная устойчивость коллоидных систем обуславливается термодинамическими и кинетическими факторами. Термодинамические факторы, действие которых направлено на снижение поверхностного натяжения и увеличение энтропии, уменьшают вероятность эффективных соударений между частицами, создают потенциальные барьеры. Кинетические факторы снижают скорость столкновения частиц и связаны в основном с гидродинамическими свойствами системы.
Различают следующие факторы устойчивости (стабилизации) дисперсных систем.
1. Электростатический фактор (термодинамический); заключается в уменьшении поверхностного натяжения вследствие возникновения двойного электрического слоя на поверхности частиц в соответствии с уравнением Липпмана. 2. Адсорбционно-сольватный фактор (термодинамический); состоит в уменьшении поверхностного натяжения в результате взаимодействия частиц с дисперсной средой (уравнение Дюпре) или благодаря адсорбции стабилизаторов (адсорбционное уравнение Гиббса). 3. Энтропийный фактор (термодинамический); проявляется в стремлении дисперсной фазы к равномерному распределению по объёму систему под действием теплового движения. 4. Структурно-механический фактор (кинетический); связан с тем, что на разрушение пленок, образующихся на поверхности частиц и обладающих упругостью и механической прочностью, требуется энергия и время. 5. Гидродинамический фактор (кинетический); заключается в снижении скорости движения частиц при изменении вязкости и плотности дисперсионной среды. 6. Смешанные факторы наиболее характерны для реальных систем; агрегативная устойчивость обеспечивается действием нескольких факторов одновременно.
Каждому фактору устойчивости соответствует специфический метод его нейтрализации. Например, электростатический фактор очень чувствителен к введению электролитов. Действие структурно-механического фактора можно предотвратить с помощью веществ, разжигающих упругие структурированные слои на поверхности частиц, а также механическим, термическим способами и др.
Устойчивость дисперсных систем определяется балансом энергии притяжения и энергии отталкивания между частицами. По теории ДЛФО (Дерягина, Ландау, Фервея, Овербека), учитывающей только электростатическую составляющую расклинивающего давления (давления отталкивания), энергия отталкивания убывает с расстоянием по экспоненциальному закону.
Для области малых электрических потенциалов суммарная энергия взаимодействия частиц (пластин) равна
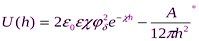
где φδ – электрический потенциал диффузного слоя; χ – величина, обратная толщине диффузного слоя; А* - константа Гамакера; h – расстояние между частицами (пластинами); ε – диэлектрическая проницаемость дисперсной среды; ε0 – электрическая постоянная.
При больших потенциалах и расстояниях между частицами (пластинами) эта энергия определяется уравнением
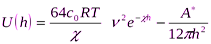
Суммарная потенциальная энергия взаимодействия частиц отрицательна на близких и далеких расстояниях (преобладает энергия притяжения). Она может быть положительна на средних расстояниях (преобладает энергия отталкивания). Максимум потенциальной кривой (рис 1.) отвечает потенциальному барьеру ΔЕ. Первый минимум I соответствует непосредственному соприкосновению частиц, а второй II – притяжению частиц, между которыми имеются прослойки среды.
Коагуляция гидрофобныхдисперсных систем может происходить в результате различных внешних воздействий, например при механическом воздействий (ультразвука), действии электрического поля, при нагревании или замораживании системы. Коагуляция гидрофобных золей может быть вызвана также их сильным разбавлением или концентрированием. Наиболее часто коагуляция дисперсных систем происходит при добавлении электролитов. Различают два типа электролитной коагуляции коллоидных систем: 1) нейтрализационную, происходящую в результате снижения поверхностного потенциала частиц; 2) концентрационную, протекающую вследствие сжатия диффузной части двойного электрического слоя (потенциал поверхности в этом случае не изменяется).
Нейтрализационная электролитическая коагуляция характерна для коллоидных систем, содержащих слабо заряженные частицы. Концентрационная коагуляция обычно наблюдается в сильно заряженных дисперсных системах.
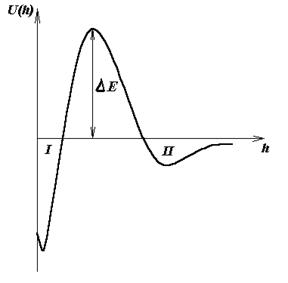
Рис.1. Зависимость энергии взаимодействия U двух частиц от расстояния между ними h.
.
Введение электролитов снижает высоту потенциального барьера, но при небольших концентрациях электролита энергетический барьер остается достаточно велик и коагуляция не происходит. Агрегация наступает при введении определенного для данной системы количества электролита, соответствующего порогу коагуляции. Порок быстрой коагуляции ск определяет количество электролита, необходимое для коагуляции единицы объёма коллоидной системы при полном исчезновении потенциального барьера ΔЕ. При сохранении небольшого потенциального барьера в системе протекает медленная коагуляция.
При электролитной коагуляции по концентрационному механизму (для сильно заряженных частиц) порок коагуляции ск в соответствии с правилом Дерягина-Ландау (обоснование эмпирического правила Шульца-Гарди) обратно пропорционален заряду z противоионов в шестой степени, т. е.
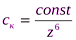
При нейтрализационной коагуляции (при малых потенциалах поверхности φ0 частиц) показатель степени z в уравнении уменьшается до двух (правило Эйлерса-Корфа).
Строение коллоидной мицеллы схематически может быть изображено на примере мицеллы иодида серебра:
{[(AgI)n mI-] xK+} (m-x)K+
| Агрегат или кристаллик твердого вещества | Потенциалопределяющие ионы | Ионы адсорбционного слоя | Ионы диффузного слоя |
ядро
частица
мицелла
 2015-08-13
2015-08-13 4310
4310