| Органы и ткани | Содержание белка, % | |
| от сухой ткани | от общего белка тела | |
| Скелетные мышцы | 34,7 | |
| Кожа | 11,5 | |
| Кости (твердые ткани) | 18,7 | |
| Пищеварительный тракт | 1,8 | |
| Мозг и нервная ткань | 2,0 | |
| Печень | 3,6 | |
| Сердце | 0,7 | |
| Легкие | 3,7 | |
| Селезенка | 0,2 | |
| Почки | 0,5 | |
| Поджелудочная железа | 0,1 | |
| Жировая ткань | 6,4 | |
| Остальные ткани: | ||
| жидкие | 1,4 | |
| плотные | 14,6 | |
| Все тело | 100,0 |
Количественный и качественный состав отдельных белков различен. Все белки содержат постоянное количество азота, равное в среднем 16%. Поэтому по количеству азота, поступившего с пищей (процентное содержание азота пищи умножают на пересчетный коэффициент 6,25), определяют потребление белка организмом.
Аминокислотный состав. Белки состоят из аминокислот. Известно около 200 различных аминокислот, однако для построения белков в животных и растительных тканях используются только 20. Называются эти аминокислоты основными.
Наряду с основными в состав отдельных белков входят другие аминокислоты — неосновные. Каждая такая аминокислота происходит от одной из 20 основных аминокислот. Например, 4-гидроксипролин и 5-дигидро-ксилизин являются производными пролина и лизина и входят в состав коллагена — белка соединительной ткани:
Простые и сложные белки. В зависимости от химического состава белки делятся на простые и сложные. Простые белки состоят только из аминокислот, среди которых есть растворимые в воде (гистоны, альбумины, фибриноген) и не растворимые (глобулины, миозин, коллаген, осеин, кератин). Сложные белки состоят из белковой и небелковой частей. Небелковая часть может быть представлена углеводами, нуклеиновыми кислотами, липидами, фосфорной кислотой, окрашенными (хромо-) веществами. В зависимости от природы небелковой части сложные белки делятся на гликопротеиды, нуклеопротеиды, липопротеиды, фосфопротеиды, хромопротеиды. Все они выполняют разнообразные функции в организме.
Биологические функции белков
• Структурная(пластическая). В комплексе с липидами белки составляют структуру всех клеточных мембран и основу цитоплазмы клеток. Структурной основой соединительной ткани являются такие белки, как коллаген (входит в состав хрящей и сухожилий), кератин (входит в состав кожи), эластин (входит в состав связок и стенок сосудов).
• Каталитическая. Эту функцию выполняют специфические белки-ферменты, регулирующие обмен веществ и энергии в организме. Если ферменты не работают в клетке, то биохимические реакции не протекают и живая клетка может погибнуть.
• Сократительная. Все виды сокращения и движения скелетных мышц, миокарда и других сокращающихся тканей обеспечивают сократительные белки актин и миозин.
• Транспортная. Белки способны связывать и транспортировать с током крови или через клеточные мембраны отдельные молекулы и ионы. Например, гемоглобин эритроцитов крови переносит кислород от легких к тканям и углекислый газ — от тканей к легким; миоглобин мышц переносит кисло род в мышечной ткани к местам его использования. Отдельные белки кро ви транспортируют жирные кислоты, липиды, железо, некоторые гормоны.
• Защитная. Белки иммунной системы гаммаглобулины "узнают" и связывают чужеродные вещества, поступающие в организм, защищая тем самым его от вирусов, бактерий и клеток других организмов. Защитную функцию выполняет также белок интерферон. Белки плазмы крови фибриноген и тромбин участвуют в процессах свертывания крови, предотвращая кровопотери при ранениях.
• Гормональная, или регуляторная. Высокоспецифические белки-гормоны регулируют обмен веществ.
• Рецепторная. Многие белки являются рецепторами гормонов, нейро- медиаторов, других биологически активных веществ. Они осуществляют избирательное узнавание, связывание и передачу их регуляторного действия.
• Передача наследственной информации. Белки входят в состав хромосом и участвуют в воспроизведении генетической информации, в регуляции процессов роста и размножения.
• Опорная. Упругость и прочность костей скелета, кожи, сухожилий обеспечивают преимущественно белки коллаген и эластин.
• Энергетическая. Около 10—15% энергопотребления организма обеспечивается белками. При окислении 1 г белков выделяется 17 кДж (4,1 ккал) энергии.
 Аминокислоты
Аминокислоты
При нагревании белков до высоких температур с крепкими кислотами, щелочами, а также под действием ферментов белковые молекулы расщепляются на более. простые соединения. На основании изучения конечных продуктов гидролиза белков было найдено, что в состав молекулы входит до 20 различных аминокислот. Аминокислотами называют соединения, содержащие одновременно аминные и карбоксильные группы. Молекулы большинства природных аминокислот имеют общую структуру, в которой аминогруппа находится в альфа-положении по отношению к карбоксильной:
Следовательно, аминогруппа присоединена к ближайшему от карбоксила углеродному атому. Некоторые аминокислоты имеют аминогруппу в бета- или -гамма-положении.
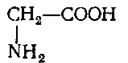 | 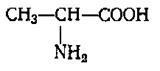 | 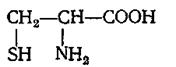 | |||
Глицин Аланин Цистеин
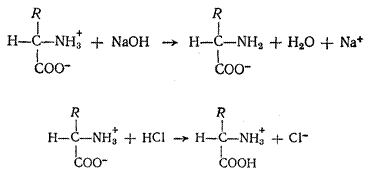
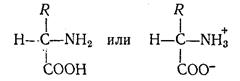 Аминокислоты являются амфотерными электролитами, т. е. обладают свойствами кислот и оснований и могут реагировать как с основаниями, так и кислотами:
Аминокислоты являются амфотерными электролитами, т. е. обладают свойствами кислот и оснований и могут реагировать как с основаниями, так и кислотами:
 |
 2015-10-14
2015-10-14 1492
1492








