Реакция с хлоридом железа (III). От прибавления раствора хлорида железа (III) к салициловой кислоте жидкость приобретает сине-фиолетовую окраску.
Реакция образования метилсалицилата. При нагревании салициловой кислоты с метиловым спиртом в присутствии серной кислоты образуется метиловый эфир салициловой кислоты (метилсалицилат):
К сухому остатку хлороформной вытяжки прибавляют 2 капли метилового спирта и 2 капли концентрированной серной кислоты. Содержимое пробирки нагревают на водяной бане. Появление характерного запаха метилсалицилата указывает на наличие салициловой кислоты в исследуемой пробе.
Обнаружение салициловой кислоты по УФ- и ИК-спектрам. Салициловая кислота в 0,5 н. растворе гидроксида натрия имеет максимум поглощения при 300 нм, а в 0,1 н. растворе серной кислоты — при 302 нм; в ИК-области спектра салициловая кислота (диск с бромидом калия) имеет пики при 1657, 1446, 1288 и 758 см -1.
Бензойная кислота — белые кристаллы, плохо растворимые в воде, хорошо — в щелочах, этаноле, хлороформе и диэтиловом эфире. Бензойная кислота является, подобно большинству других органических кислот, слабой кислотой.
Раздражает кожу; вдыхание аэрозоля вызывает судорожный кашель, насморк, иногда тошноту и рвоту.
Реакция с хлоридом железа (III). Растворяют 0,01 г бензойной кислоты на часовом стекле в нескольких каплях раствора аммиака и выпаривают на водяной бане досуха. Остаток растворяют в воде и прибавляют 1 каплю сильно разведенного раствора хлорного железа. Выпадает буровато-желтый осадок.
Осторожно нагревают пробу препарата со спиртом и концентрированной серной кислотой. Обнаруживается характерный запах бензойноэтилового эфира.
39.Алкалоиды - производные пиридина и пиперидина: никотин, анабазин, пахикарпин. Характеристика. Реакции обнаружения, методы количественного определения.
Анабазин — алкалоид, содержащийся в ежевнике безлистном. Небольшие количества анабазина содержатся в табаке. Основание анабазина представляет собой бесцветную маслянистую жидкость, которая хорошо растворяется в воде и ряде органических растворителей.
В малых дозах анабазин возбуждает центральную нервную систему, усиливает дыхание, повышает кровяное давление, возбуждает ганглии вегетативной нервной системы. В больших дозах анабазин оказывает угнетающее и парализующее действие вегетативных ганглиев. Анабазин проникает в организм с вдыхаемым воздухом, а также через неповрежденную кожу и может давать тяжелые отравления. Выделяется из организма с мочой. Метаболизм анабазина изучен недостаточно.
Для выделения анабазина применяют метод, основанный на изолировании алкалоидов водой, подкисленной серной кислотой, а также метод перегонки с водяным паром.
Один из методов выделения анабазина основан на том, что биологический материал настаивают с водой, подкисленной серной кислотой. Полученную кислую вытяжку фильтруют или центрифугируют, подщелачивают и взбалтывают с хлороформом или другими органическими растворителями, в которые переходит основание анабазина.
Реакция с реактивом Драгендорфа. На предметное стекло наносят 2—3 капли хлороформного раствора исследуемого вещества и выпаривают досуха. К сухому остатку прибавляют каплю 0,1 н. раствора соляной кислоты и каплю реактива Драгендорфа. Предметное стекло вносят во влажную камеру (см. гл. 3, § 2) на 20—30 мин, а затем продукт реакции рассматривают под микроскопом. Появление сростков, состоящих из оранжево-красных кристаллов, имеющих игольчатую форму, указывает на наличие анабазина в исследуемом растворе.
Реакция с пикриновой кислотой. К капле исследуемого раствора прибавляют 2 капли насыщенного раствора пикриновой кислоты. При наличии анабазина в растворе выпадает желтый кристаллический осадок. Никотин не дает этой реакции.
Реакция с реактивом Бушарда. К 2—3 каплям исследуемого раствора прибавляют каплю реактива Бушарда. При наличии анабазина выпадает красно-бурый осадок. Эту реакцию дает и никотин.
Реакция с пергидролем. В пробирку вносят 1 мл исследуемого раствора, 1 мл пергидроля и 2—3 капли концентрированной серной кислоты. Появление красной или шоколадно-коричневой окраски указывает на присутствие анабазина в растворе. Эту реакцию дает и никотин.
Никотин — бесцветная маслянистая жидкость (т. кип. 247,6 °С), быстро темнеющая на воздухе. При температурах ниже 60 °С и выше 210 °С никотин смешивается с водой, а в интервале температур от 60 °С до 210 °С он ограниченно растворяется в воде. Никотин хорошо растворяется во многих органических растворителях.
Он поражает центральную и периферическую нервную систему. Особенно характерным является действие никотина на ганглии вегетативной нервной системы. После поступления в организм больших доз никотина происходит угнетение и паралич нервной системы, остановка дыхания с последующим прекращением сердечной деятельности.
Никотин быстро всасывается через слизистые оболочки рта, пищевого канала, а также через легкие. Он может поступать в организм и через неповрежденную кожу (опасно даже попадание на кожу нескольких капель никотина).
Выделение никотина из биологического материала производится так, как и выделение анабазина
Реакция с реактивом Драгендорфа. Обнаружение этого алкалоида при помощи реактива Драгендорфа производится так, как и обнаружение анабазина. При наличии никотина в исследуемом растворе после прибавления реактива Драгендорфа в поле зрения микроскопа наблюдаются сростки кристаллов в виде летящих птиц, буквы К или буквы X.
Реакция с раствором иода в диэтиловом эфире. В пробирку вносят 1 мл раствора исследуемого вещества в диэтиловом эфире и прибавляют 1 мл 10 %-го раствора иода в диэтиловом эфире. Через несколько минут смесь мутнеет, а затем выпадает смолистый осадок, содержащий игольчатые рубиново-красные кристаллы с темно-синим оттенком. Анабазин не дает этой реакции.
Реакция с формальдегидом. На часовое стекло или на капельную пластинку наносят 1—2 капли исследуемого раствора и 2 капли 4 %-го водного раствора формальдегида. Смесь нагревают, затем прибавляют каплю концентрированной азотной кислоты. В присутствии никотина раствор приобретает красную или розовую окраску. Анабазин не дает этой реакции.
Другие реакции на никотин. Никотин можно обнаружить при помощи реакций с реактивом Бушарда, раствором ванилина и пергидролем. Выполнение этих реакций приведено при описании способов обнаружения анабазина.
Обнаружение никотина по УФ-спектрам. Никотин в 0,1 н. растворе серной кислоты имеет максимум поглощения при 260 нм.
Пахикарпин представляет собой почти бесцветнe. Густe. маслообразную жидкость, быстро темнеющую на воздухе. В медицине применяется гидроиодид пахикарпина. Это белый кристаллический порошок, растворимый в воде, этиловом спирте и хлороформе, слаборастворимый в диэтиловом эфире и ацетоне.
Пахикарпин не кумулируется в организме. Уже через 6 ч после приема пахикарпина его можно обнаружить в неизмененном виде в моче. За сутки пахикарпин почти полностью выводится из организма. В результате приема больших доз пахикарпина могут быть отравления, признаки которых появляются через 1—3 ч. Наступает тошнота, рвота, головокружение, затрудненное дыхание, помрачнение сознания. Отмечается расширение зрачков, цианоз, могут появиться судороги и др. Смерть наступает от асфиксии.
Реакция с роданидом кобальта. Пахикарпин с роданидом кобальта дает кристаллический осадок.
Реакция с пикриновой кислотой. Пахикарпин с 0,5 %-м раствором пикриновой кислоты образует кристаллический осадок (сростки из желто-зеленых призматических кристаллов).
40.Алкалоиды - производные тропана: атропин, скополамин, кокаин. Характеристика. Реакции обнаружения, методы количественного определения.
Атропин представляет собой сложный эфир тропина и троповой кислоты. Основание атропина растворяется в хлороформе, диэтиловом эфире, этиловом спирте, хуже растворяется в воде. Сульфат атропина растворяется в воде, этиловом спирте, практически не растворяется в диэтиловом эфире и хлороформе.
Атропин быстро всасывается через слизистые оболочки, кожу, кишки (но не через желудок). Принятая доза атропина почти полностью всасывается в тонкой кишке в течение двух часов. Примерно половина поступившего в организм атропина циркулирует в крови, а вторая — связывается с белками плазмы.
Обнаружение атропина
Реакции с реактивами группового осаждения алкалоидов.
Атропин дает осадки с реактивами Бушарда, Драгендорфа, Майе-ра и др.
Реакция Витали — Морена. Эта реакция основана на том, что при нагревании атропина с азотной кислотой он разлагается на тропин и троповую кислоту. При действии азотной кислоты на троповую кислоту образуется тринитропроизводное этой кислоты, имеющее желтую окраску.
Реакция с пикриновой кислотой. Атропин с 0,5 %-м раствором пикриновой кислоты дает светло-желтый кристаллический осадок в виде пластинок или сростков из них. Этот осадок появляется через 15—20 мин.
Реакция с п -диметиламинобензальдегидом и серной кислотой. К 2—3 каплям исследуемого раствора прибавляют 3—5 капель 0,5 %-го раствора п -диметиламинобензальдегида в концентрированной серной кислоте. Жидкость взбалтывают, а затем нагревают на кипящей водяной бане 5—10 мин. При наличии атропина появляется красная окраска, которая переходит в вишнево-красную, а затем в фиолетовую.
Скополамин является сложным эфиром скопина и троповой кислоты. Основание скополамина кристаллизуется с одной молекулой воды. Образующийся моногидрат основания скополамина плавится при 59 °С. Гидробромид скополамина растворяется в воде, этиловом спирте, практически не растворяется в диэтиловом эфире и хлороформе.
Скополамин легко всасывается через пищеварительный тракт. Поступивший в организм скополамин связывается с белками плазмы крови, а небольшое количество принятой дозы подвергается гидролизу. Основное количество скополамина разлагается в печени и выводится из организма с мочой.
Скополамин дает большинство реакций, которые используются для обнаружения атропина (реакция Витали — Морена, реакция с п -диметиламинобензальдегидом и солью Рейнеке).
Скополамин и атропин можно отличить друг от друга при, помощи реакции образования бромаурата скополамина, а также при помощи метода хроматографии и на основании спектров в ИК-области.
Кокаин является алкалоидом, который находится в листьях кока. По химическому строению кокаин представляет собой метиловый эфир бензоилэкгонина. Основание кокаина растворяется в хлороформе, диэтиловом эфире, этиловом спирте, плохо растворяется в воде.
В определенных дозах он вызывает эйфорию, возбуждение, а затем угнетение центральной нервной системы. При частом приеме кокаина к нему развивается болезненное пристрастие (кокаинизм).
Метаболизм. Кокаин в основном метаболизируется в печени. Образующиеся при этом метаболиты выделяются с мочой. При гидролизе кокаина образуется метиловый спирт и бензоилэкгонин, который превращается в экгонин и бензойную кислоту. Экгонин быстро разлагается в организме, поэтому его трудно обнаружить в моче.
Обнаружение кокаина
Реакция с реактивами группового осаждения алкалоидов. Кокаин дает осадки с реактивами Майера, Бушарда, Драгендорфа, пикриновой кислотой и др.
Реакция с перманганатом калия. Появляются красно-фиолетовые кристаллы, имеющие форму прямоугольных пластинок и сростков из них. С перманганатом калия кристаллические осадки дают скополамин, аконитин, тропакокаин, котарнин, берберин и гидрастин. Однако форма кристаллов этих веществ с перманганатом калия отличается от формы кристаллов кокаина с указанным реактивом.
Реакция с платинохлористоводородной кислотой. К сухому остатку, полученному после выпаривания хлороформного раствора, прибавляют каплю 0,1 н. раствора соляной кислоты и каплю 10%-го раствора платинохлористоводородной кислоты. При наличии кокаина образуются светло-желтые кристаллы, имеющие форму перистых дендритов.
41.Производные барбитуровой кислоты: барбитал, фенобарбитал, барбамил, бутобарбитал, бензонал. Характеристика. Реакции обнаружения, методы количественного определения.
Для выделения барбитуратов из биологического материала долгое время применялись методы, которые были разработаны для выделения алкалоидов. В последние десятилетия для выделения барбитуратов из объектов биологического происхождения предложен ряд специальных методов, которые описаны ниже.
Для обнаружения барбитуратов применяются цветные реакции, реакции осаждения, микрокристаллоскопические реакции, методы хроматографии, УФ- и ИК-спектроскопии и др.
Реакции обнаружения производных барбитуровой кислоты.
1.1.1. Реакция выделения кислотной формы барбитуратов На предметное стекло наслаивают несколько капель исследуемого раствора. Сухой остаток растворяют в капле концентрированной серной кислоты. Через 3-5 минут рядом помещают каплю дистиллированной воды, осторожно соединяют обе капли. Через 30-60 минут наблюдают появление кристаллического осадка, характерного для каждого отдельного барбитурата.
Частные реакции.
1.2.2. Реакция с железойодидной комплексной солью.
При наличии фенобарбитала наблюдаются призматические кристаллы и сростки из них оранжево-коричневого цвета.
При наличии барбамила наблюдаются крупные призматические кристаллы и сростки из них розово-оранжевого цвета в виде бабочек.
При наличии этаминала-натрия наблюдаются мелкие пластинчатые призматическиме кристаллы и сростки из них коричневного цвета.
Другие барбитураты либо не дают кристаллических осадков с этим реактивом, либо образуют кристаллы нехарактерной формы.
1.2.3. Реакция с меднойодидной комплексной солью.
Меднойодидная комплексная соль дает с барбамилом и этаминалом кристаллические осадки, аналогичные тем, какие образует железойодидная соль. Условия выполнения реакций такие же, как и с железойодидной комплексной солью.
1.2.4. Цветной тест. На фильтровальную бумагу в одну точку нанести 2-3 капли раствора барбитурата в органическом растворителе или кислого извлечения, подсушить, затем наслоить 1-3 капли 1% спиртового раствора кобальта нитрата Со(NO3)2, подсушить и внести бумагу в пары 25% раствора аммиака – пятно приобретает красно-фиолетовое окрашивание.
1.2.5. Мурексидная реакция. В фарфоровую чашку к сухому остатку, полученному после выпаривания части извлечения, добавить по 3 капли 3% раствора перекиси водорода и реактива, содержащего соль Мора и хлорид аммония. Содержимое чашки выпарить, сухой остаток нагреть до появления белых паров. После охлаждения добавить 3 капли 6 н. раствора аммиака. При наличии некоторых барбитуратов и тиобарбитуратов появляется розовая окраска.
Мурексидную реакцию дают барбамил, барбитал, фенобарбитал, этаминал-натрий и тиопентал. Не дают этой реакции гексенал, гексобарбитал и циклобарбитал.
УФ-спектрометрический анализ барбитуратов позволяет одновременно с качественными характеристиками (максимумы поглощения) получить данные для расчета количественного содержания веществ.
42.Алкалоиды – производные пурина: кофеин, теобромин. Характеристика. Реакции обнаружения, методы количественного определения.
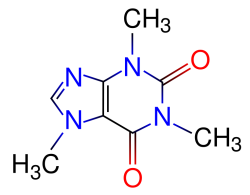 - кофеин явл-ся алкалоидом, к-ый сод.в кофе, чае и нек-ых др.растениях. Экстрагируется орг-ми р-ми из кислых и частично из щелочных р-ров. Р-ции обнаружения. 1. Мурексидная р-ция: нес-ко капель хлороформного р-ра исслед-го в-ва помещают в фарф.чашечку,и р-ль испаряют без нагревания. К сух.остатку приб. Насыщ.р-р бромной воды и выпаривают на вод.бане досуха. К окрашенному в буроватый цвет остатку подносят на стеклянной палочке 25% р-ра аммиака. Остаток приобретает пурпурно-фиолет.окрашивание. 2.Дает осадки с реакт.Драгендорфа, Зонненшейна, Шейблера и др. 3.Р-ция с реат.Несслера. При нагревании р-ра с реактивом появл. Красно-бурый осадок. 4.Р-ция с ртути(II)хлоридом: на предм.стекло наслаивают капли исслед-го хлороформного р-ра. На сухой остаток после удаления хлороформа наносят каплю р-ра НСI и 5% р-р ртути (II)хлорида, обр-ся крупные,шелковистые,б\цв иглообразные кристаллы.
- кофеин явл-ся алкалоидом, к-ый сод.в кофе, чае и нек-ых др.растениях. Экстрагируется орг-ми р-ми из кислых и частично из щелочных р-ров. Р-ции обнаружения. 1. Мурексидная р-ция: нес-ко капель хлороформного р-ра исслед-го в-ва помещают в фарф.чашечку,и р-ль испаряют без нагревания. К сух.остатку приб. Насыщ.р-р бромной воды и выпаривают на вод.бане досуха. К окрашенному в буроватый цвет остатку подносят на стеклянной палочке 25% р-ра аммиака. Остаток приобретает пурпурно-фиолет.окрашивание. 2.Дает осадки с реакт.Драгендорфа, Зонненшейна, Шейблера и др. 3.Р-ция с реат.Несслера. При нагревании р-ра с реактивом появл. Красно-бурый осадок. 4.Р-ция с ртути(II)хлоридом: на предм.стекло наслаивают капли исслед-го хлороформного р-ра. На сухой остаток после удаления хлороформа наносят каплю р-ра НСI и 5% р-р ртути (II)хлорида, обр-ся крупные,шелковистые,б\цв иглообразные кристаллы.
Кофеин является алкалоидом, который содержится в кофе, чае и некоторых других растениях Кофеин изолируется из биологического материала по общему ходу химико-токсикологического анализа как подкисленным спиртом, так и подкисленной водой, а затем извлекается хлороформом из кислого раствора Еще легче извлекается хлороформом из растворов, подщелоченных аммиаком, если он не был предварительно извлечен из кислых растворов. Максимум экстракции хлороформом наблюдается при рН 4,0-7,0.. Реакции обнаружения 1. Мурексидная реакция 5 – 6 капель хлороформного раствора ЛП помещают в фарфоровую чашечку, и растворитель испаряют без нагревания. СУХ ОСТ+ бромной воды и выпаривают на водяной бане досуха.+ 25% раствора аммиака. Остаток в чашке при наличии кофеина приобретает пурпурно–фиолетовое окрашивание. 2. Кофеин даёт осадки с реактивами Драгендорфа, Зонненшейна, Шейблера и др.3. Реакция с реактивом Несслера
При нагревании раствора с реактивом Несслера (на кипящей водяной бане) в течение 1 – 2 мин появляется красно–бурый осадок.4. Реакция с ртути (II) хлоридом.. На сухой остаток после удаления хлороформа наносят каплю хлороводородной кислоты и каплю 5% раствора ртути (II) хлорида, через 10 – 15 мин образуются крупные, шелковистые, бесцветные иглообразные кристаллы.
Токсикологическое значение. Кофеин может вызывать отравление, иногда даже со смертельным исходом. Действие кофеина на организм многосторонне. Избирательно он действует на центральную нервную систему и в первую очередь на кору головного мозга. Работами школы И. П. Павлова доказано, что кофеин усиливает процесс возбуждения коры головного мозга. Из организма кофеин выводится быстро. Кумулятивными свойствами не обладает. Патологоанатомические изменения при отравлениях не наблюдаются. В практике химико-токсикологического анализа с кофеином приходится чаще встречаться не как с ядом, а как с широко распространенным лекарственным препаратом
43.Производные п -аминобензойной кислоты: новокаин, новокаинамид. Характеристика. Реакции обнаружения, методы количественного определения.
Новокаин (прокаин, аллокаин, синкаин и др.) — гидрохлорид β -диэтиламиноэтилового эфира п -аминобензойной кислоты. Он представляет собой белый кристаллический порошок без запаха. Растворяется в воде, этиловом спирте, слабо растворяется в диэтиловом эфире и хлороформе. Новокаин экстрагируется органическими растворителями из щелочных водных растворов.
Обнаружение новокаина. Для обнаружения новокаина применяют реакцию диазотиро-вания, реакцию с реактивом Драгендорфа и физико-химические методы.
Реакция диазотирования. К исследуемому раствору прибавляют 1 %-й раствор соляной кислоты, а затем по каплям прибавляют 1 %-й раствор нитрита натрия до тех пор, пока не начнет окрашиваться в синий цвет иодкрахмальная бумажка. Через 5 мин жидкость подщелачивают 2%-м раствором гидроксида натрия до щелочной реакции и прибавляют щелочной раствор β-нафтола. При наличии новокаина раствор приобретает красно-оранжевую окраску.
 2018-01-21
2018-01-21 2331
2331








