В технологических расчётах добычи и транспорта газа часто пользуются основными термодинамическими характеристиками природного газа: теплоёмкостью, энтропией, энтальпией, теплотой сгорания, теплообменом, теплопроводностью.
Теплоёмкость. Теплоёмкостью называют количество теплоты, необходимое для нагревания единицы массы или объёма вещества на 1° С.
Отношение теплоёмкости в массе системы М называется удельной теплоёмкостью:
с = С/М, (31)
а отношение теплоёмкости к количеству вещества – молярной теплоемкостью:
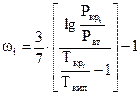 (27)
(27)
где Рат - атмосферное давление;
Ткип - температура кипения компонента при атмосферном давлении.
Ацентрический фактор для многих веществ изменяется от 0,0 до 0,4. Отношение абсолютной критической температуры компонента к абсолютной температуре кипения (при нормальных физических условиях) зависит от типа углеводородов - парафиновых, нафтеновых или ароматических. Для углеводородов парафинового ряда это отношение можно определить, например, по корреляционной зависимости Г. Р. Гуревича
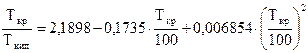 (28)
(28)
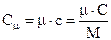 . (32)
. (32)
Единицей количества теплоты, работы, энергии в системе СИ является джоуль (Дж). Джоуль - работа силы 1 Н при перемещении ею тела на расстоянии 1 м в направлении действия силы:
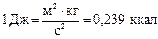
Теплоёмкость выражается в Дж/К, удельная теплоёмкость – в Дж/(кг·K), молярная теплоёмкость – в Дж/(моль К).
Теплоёмкость природных газов зависит от химического состава и состояния, а также от процесса сообщения им теплоты. В адиабатическом процессе С = 0, в изобарическом С = Ср, в изохорическом С = Сv.
Для газов обычно различают теплоёмкости при постоянном объёме Сv и постоянном давлении Ср.
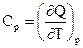
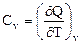 (33)
(33)
где Р = const и V = const.
Сv связана с процессом, характеризующимся тем, что при неизменности объёма вся энергия, сообщаемая газу в форме теплоты, затрачивается на увеличение внутренней энергии газа. Ср связана с процессом, характеризующимся тем, что, нагревая тело, предоставляют ему возможность расширяться при неизменном давлении. Таким образом, часть сообщенной телу теплоты идет на производство работы расширения. Поэтому Ср > Сv.
Для идеальных газов между Ср и Сv существует следующее соотношение в [кал/моль·°С]:
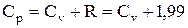 (34)
(34)
где R - газовая постоянная.
В области давлений, где газы считаются идеальными, значения теплоёмкостей постоянны. Однако для реальных газов значения теплоёмкости изменяются в зависимости от давления. Для смеси газов теплоёмкость определяется по сумме теплоемкости входящих компонентов по формуле
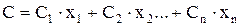 (35)
(35)
где С1, С2…Сn - теплоёмкости отдельных компонентов смеси;
х1, х2…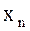 содержание компонентов в долях единицы.
содержание компонентов в долях единицы.
Отношение теплоёмкости 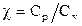 называют показателем адиабаты.
называют показателем адиабаты.
Для сравнительной характеристики различного вида топлива используется понятие удельной теплоты сгорания.
Удельной теплотой сгорания газового топлива называется количество теплоты, которое выделяется при полном сгорании 1 н.м3 или 1 кг газа. Теплоту сгорания газообразного топлива обычно измеряют в ккал/м3 при температуре 0 или 20 0С и давлении 760 мм. рт. ст. расчётным путём по известному химическому составу газа или же с помощью калориметров.
Различают низшую теплоту сгорания Qн и высшую теплоту сгорания Qв.
Высшая теплота сгорания газового топлива соответствует условию, при котором водяные пары продуктов сгорания доводятся до жидкого состояния. В реальных условиях сжигания газа водяные пары не конденсируются, а находятся в парообразном состоянии. Понятие низшей теплоты сгорания относится только к тем газам, которые при сгорании выделяют водяные пары. Разница между Qв и Qн составляет порядка 600 ккал на каждый килограмм водяных паров, т.е. 6 ккал на каждый процент влаги, содержащейся в топливе или образующийся при сгорании водорода, входящего в состав горючего газа.
 2014-02-05
2014-02-05 1070
1070








