Сопоставляя электродные потенциалы j0Zn/Zn2+ = –0,76 В и j0Fe/Fe2+= –0,44 В, видим, что j0Zn < j0Fe.Следовательно, цинк по отношению к железу является анодом. Цинковое покрытие – анодное покрытие. На аноде идет процесс окисления:
Zn – 2ē = Zn2+.
На катоде (Fe) – процесс восстановления частиц среды (во влажном воздухе это кислород и вода):
2Н 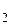 O + O
O + O 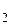 + 4ē = 4OH
+ 4ē = 4OH 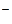 .
.
Продукты коррозии: Zn2+ + 2OH- = Zn(OH)2.
При нарушении покрытия сталь не растворяется, следовательно, цинковое покрытие использовать можно.
Толщину покрытия ∆ h можно найти из уравнения:
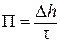 , мм/год,
, мм/год,
откуда ∆ h = П×t = 0,16.5 = 0,8 мм.
Но коррозии подвержено 82 % первоначальной толщины. Тогда вся толщина покрытия должна быть равна 100 %:
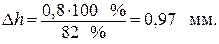
Задачи
251 – 255 Составьте электронные уравнения анодного и катодного процессов коррозии стального трубопровода (основной компонент стали – железо), содержащего примеси металла А, во влажной почве (присутствуют вода и кислород). Каков состав продуктов коррозии? Рассчитайте толщину стенок трубопровода (мм), который должен прослужить τ лет, если скорость его коррозии равна j. Остаточная толщина стенок трубопровода должна быть не меньше 25 % от первоначального значения. Плотность железа r = 7,87 г/см3.
|
|
|
| № задачи | Примесь А | j, кг/м2×год | t, лет | Ответ, мм |
| Ni | 3,305 | 8,4 | ||
| Sn | 6,558 | 6,67 | ||
| Pb | 4,984 | 5,07 | ||
| Cu | 1,695 | 3,73 | ||
| Sb | 6,690 | 4,53 |
256–259 Можно ли использовать предлагаемый материал в качестве протектора для защиты стального изделия от коррозии в природной воде, насыщенной кислородом (основной компонент стали – железо)? Составьте электронные уравнения анодного и катодного процессов коррозии. Каков состав продуктов коррозии? Определите возможный срок службы протектора сечением «а×в», если скорость его коррозии j, г/м2×год, а масса m, г.
| № задачи | Материал протектора | а, см | в, см | j, г/м2×год | m, г | Ответ |
| Zn | ||||||
| Al | 2,5 | |||||
| Mg | ||||||
| Zn-Hg | 8,9 |
260–262 Можно ли использовать предполагаемое покрытие для эффективной защиты стального изделия от коррозии во влажном воздухе? (Основной компонент стали – железо.)
Составьте электронные уравнения анодного и катодного процессов коррозии, возникающей при нарушении целостности покрытия. Каков состав продуктов коррозии? Какой должна быть толщина покрытия, чтобы оно прослужило τ лет, если величина его глубинного показателя П, мм/год? Покрытие считается действующим до тех пор, пока его остаточная толщина не составит 15 % от первоначального значения.
| № задачи | Материал покрытия | П, мм/год | t, лет | Ответ, мм |
| Mg | 0,7 | 3,3 | ||
| Zn | 0,3 | 1,76 | ||
| Al | 0,6 | 3,53 |
263–266 При химической коррозии металлов Ме в атмосфере сухого воздуха, содержащего газообразные O2; HCl; H2S, под воздействием высоких температур образуются пленки продуктов коррозии. Напишите уравнения образования соединений. Зная плотности металлов, их оксидов, хлоридов, сульфидов, определите, какие из пленок будут обладать защитным действием.
|
|
|
| № задачи | Металл, Ме | r 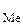 , г/см3 , г/см3 | Продукты коррозии и их плотности, г/см3 |
| Fe | 7,87 | FeO –5,7; Fe2O3 –5,25; FeCl2 – 2,9; FeS2 – 5,03; Fe3O4 – 5,18 | |
| Cu | 8,94 | CuO – 6,46; Cu2O – 3,7; CuCl2 – 3,05; Cu2S – 5,4; CuS – 4,68 | |
| Mn | 7,74 | MnO –5,18; Mn2O3 – 4,3; Mn3O4 – 7,42; MnCl2 – 2,98; MnO2 – 5,03 | |
| Ni | 8,91 | NiO – 7,45; Ni2S3 – 5,82; NiCl2 – 3,51; NiS – 4,12 |
267–270 Металлическое изделие, содержащее примесные включения А (см. таблицу), сильно корродирует в растворе HCl. Для замедления процесса в растворах кислот используют ингибиторы. Определите коэффициент торможения коррозии К и степень защиты Z, которые обеспечивает ингибитор, если за t часов потери массы изделия площадью S составляют m 0 граммов в отсутствие ингибитора и m граммов при его наличии. Составьте электронные уравнения анодного и катодного процессов коррозии изделия в кислоте. Каков состав продуктов коррозии?
| № задачи | Металл изделия | Примесь | t (час) | S (м2) | m 0 (г) | m (г) |
| Fe | Cd | |||||
| Fe | Ni | 70,8 | ||||
| Zn | Bi | |||||
| Cr | Sn |
Ответ: 267) 3,5; 71,2 %; 268) 8,0; 87,6 %; 269) 8,0; 87,6 %; 270) 2,6; 61,6 %.
 2015-02-27
2015-02-27 1071
1071








