А14. В схеме превращений А 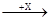 FeCl3
FeCl3 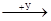 А
А 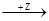 FeCl2 все реакции окислительно-восстановительные. Определите возможные реагенты А,Х,У и Z.
FeCl2 все реакции окислительно-восстановительные. Определите возможные реагенты А,Х,У и Z.
1) A – Fe, X – Cl2, У – Mg, Z – CuCl2
2) A – Fe(OH)3, X – HCl, У – NaOH, Z – HCl
3) A – Fe2O3, X – Cl2, У – AgNO3, Z – BaCl2
4) A – Fe(OH)2, X – HCl, У – КOH, Z – Cl2
Решение:
1) 2Fe0 + 3CI20 → 2Fe+3CI-13
A X
2Fe+3CI-13 + 3Mg0 → 3Mg+2CI2 + 2Fe0
Y A
Fe0 + Cu+2CI2 → Fe+2CI2 + Cu0
A Z
Ответ: 1
А15. Количество возможных окислительно-восстановительных реакций между веществами – Zn, AgNO3(p-p), Cu, Pb(NO3)2(p-p), Cr2O3, – в результате которых можно получить простое вещество металл, равно:
1) 4 2) 3 3) 2 4) 1
Решение:
Более активные металлы (расположенные левее в электрохимическом ряду напряжений металлов) вытесняют менее активные металлы их растворов их солей
1) Zn + 2AgNO3 = Zn(NO3)2
2) Zn + Pb(NO3)2 = Zn(NO3)2 + Pb
3) Cu + 2AgNO3 = Cu(NO3)2 + 2Ag↓
 2015-03-08
2015-03-08 816
816








