| R-Стадия | 5.60 | D/A Ratio: 0.33 | |
| А-Стадия | 9.47 | С/В Ratio: 4.13 | |
| В-Стадия | 1.58 | ||
| С-Стадия | 6.55 | Классификация: | |
| D-Стадия | 3.15 | В — Стадия метаболических нарушений |
Рис. 4.14. Вид документа после окончания расчетов.
Расчет дистанций до каждого из кластеров позволяет определить минимальную, которая и выносится в качестве заключения о конкретном состоянии.
Следует заметить, что информативность полученного заключения проявляется не в полной мере, поскольку анализ динамики процесса требует ориентации в четырехмерном пространстве, которое не является привычной категорией клинического мышления. Для облегчения восприятия четырехмерного пространства и для наглядной оценки динамики процесса была использована двухмерная интерпретация. С этой целью отношение расстояния до кластера С к расстоянию до кластера В откладывали по оси абсцисс, а отношение расстояния до кластера D к расстоянию до кластера А—в качестве второй из осей — оси ординат.
Выбор именно этих отношений не является случайным. В ходе патофизиологического анализа кластера С (кластер “легочно-сердечных нарушений”) было отмечено, что ведущими в формировании специфического образа этого кластера являются, вероятнее всего. нарушения вентиляционно-перфузионных взаимоотношений, что на фоне нарастающей гипоксии приводит и к развитию сердечной декомпенсации. В то же время в организме пострадавшего выраженность аэробных процессов еще достаточно велика, и это проявляется в значительном увеличении артерио-венозного градиента кислорода. низком парциальном давлении кислорода в венозной крови.
При соответствующем анализе кластера В (“метаболического дисбаланса”) было обращено внимание на резкое снижение потребления кислорода на фоне увеличения его парциального давления в венозной крови при сохраняющемся потоке, а также сужении артерио-венозного градиента кислорода. Все эти изменения отмечены на фоне увеличения отношения лактат/пируват. Это позволяет с большой степенью уверенности полагать, что для данного кластера основным признаком можно считать активацию процессов анаэробного метаболизма.
Введение в практику отношения расстояния до кластера С к расстоянию до кластера В позволит уже по его величине ориентировочно судить о взаимоотношении аэробного и анаэробного путей метаболизма.
Как следует из проведенного анализа кластера А (кластер гипердинамической реакции или “стрессового ответа”), в основе его патофизиологических проявлений лежит прежде всего нарушение системной регуляции сосудистого тонуса, что и вызывает резкое увеличение производительности сердца и. для компенсации, увеличение объема сосудистого русла. При изучении патофизиологических особенностей кластера D (“гиповолемические нарушения”) ведущим является снижение насосной функции сердца, компенсация которой обеспечивается значительным повышением сосудистого тонуса. В то же время ни в одном из этих кластеров не определяется повышения уровня анаэробного метаболизма. С другой стороны, это отношение связано функциональной зависимостью с развивающимся метаболическим дисбалансом, так как его диспропорциональность, по одной из гипотез. обусловлена в значительной степени дефектом утилизации ароматических аминокислот и синтезом “фальшивых нейротрансмиттеров” [34]. В соответствии с этим по отношению расстояния до кластера D к расстоянию до кластера А можно уже в общих чертах судить о состоянии сосудистого тонуса и насосной функции сердца.
Таким образом, дистанции от конкретного профиля пациента до всех патологических и контрольного профилей после их преобразовании выражаются в виде трех чисел: два отношения — D/A и С/В и расстояние до контрольной группы.
Получаемое графическое отображение динамики указанных показателей у больного в сопоставлении с имеющимися клиническими данными позволяет судить о нарастании тех или иных патологических процессов, а также определять в некоторой мере адекватность ответа организма пострадавшего на развитие патологического процесса. В качестве иллюстрации приводится график динамики одного из больных, вошедших в наше исследование (рис. 4.15). На представленном графике видно, что по оси абсцисс отложены значения отношения С/В, а по оси ординат соответствующие значения D/A. Динамика состояния больного определена в виде траектории — ломаной линии. соединяющей точки, в которых определялись показатели системы функционального компьютерного мониторинга и рассчитывались соответствующие значения отношений С/В и D/A. Рядом с точками забора указан последовательный номер пробы, а в скобках — типичный патофизиологический профиль, дистанция до которого была в момент данного исследования минимальной.
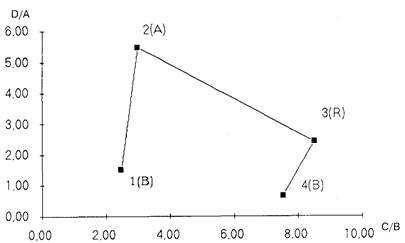
Рис. 4. 15. Схематическое отображение динамики опенки состояния по системе функционального компьютерного мониторинга у больного К.
Таким образом, в настоящей главе представлена методика разработки и патофизиологического обоснования типичных патологических профилей у пострадавших с тяжелой механической травмой, которые могут рассматриваться в качестве основных клинических образов течения постшокового периода. Их использование позволяет исследовать математически динамику состояния каждого конкретного пострадавшего в соответствии с его показателями в разработанной на этой основе системе функционального компьютерного мониторинга и оценить количественно и качественно выраженность патологических процессов.
В ходе дальнейшего изучения типовые кластеры (паттерны) А, В, С, D, идентифицированные по блоку исследований, относящихся к определенному периоду развития процесса у конкретною больного, нередко обозначаются как фазы А, В, С или D. Такое обозначение нам представляется корректным, поскольку под фазой понимается конкретный этап развития патологического процесса, выделенный на основе сопряженного анализа клинических признаков и патофизиологических механизмов.
РЕЗЮМЕ
В настоящей главе представлено теоретическое обоснование и подробно описана методика разработки системы функционального компьютерного мониторинга у пострадавших с тяжелой механической травмой. Ее использование позволяет в любой момент времени получить количественное и качественное описание состояния больного. ориентированное на один из патологических профилей.
В ходе разработки системы убедительно подтвердилось немаловажное обстоятельство: конкретная значимость получаемой в ходе компьютерного мониторинга информации значительно возрастает, если она (система) ориентирована на распознавание узлового патогенетического звена(в нашем случае — взаимоотношение анаэробного и аэробного путей утилизации и синтеза энергетических субстратов) патологического процесса — генерализованных воспалительных осложнений. Полагая, что развитие генерализованных воспалительных осложнений тяжелых механических повреждений (читай, экстремального состояния) происходит в результате цитокиновой агрессии, которую мы в настоящее время не можем отслеживать в режиме реального времени, была предпринята попытка разработать систему. характеризующую ранние следствия этой атаки — появление метаболических нарушений. Представляется важным связать воедино клинические проявление синдрома системной воспалительной реакции и те ранние изменения метаболизма, которые нам позволяет выявить система функционального компьютерного мониторинга. По нашим представлениям, это основное направление в ранней диагностике и профилактике развивающихся генерализованных осложнений и сепсиса после тяжелых механических травм. Этому и будет посвящена следующая глава настоящей монографии.
ЛИТЕРАТУРА
1. Истратов В. Г., Жуков А.О. Новые методические подходы к оценке тяжести состояния больных хирургическим сепсисом //Междунар. конф. “Раны и раненая инфекция”.— М 1993.— С. 361—362.
2. Kавкалo Д.Н., Koновалов Е.П., Пляцок А.А. Прогнозирование и профилактика сепсиса в неотложной хирургии //Хирургия.— 1992.—№ 7—8.—С. 14—17.
3. Столбовой А.В. Квалиметрия хирургической инфекции //Междунар. конф. “Раны и раневая инфекция”.—М., 1993.— С. 432—434.
4. Цибин Ю.Н., Гальцева И. В., Рыбаков И.Р., Фролов Г.М. Балльная оценка шокогенности травмы в зависимости от их локализации и характера // Травматический шок.— Л., 1977. С. 60—62.
5. Abel F.L. Myocardial function in sepsis and endoloxin shock //Amer. J. Physiol-1989. -Vol. 257. № 6, pt. 2.- P. RI265-R12S1.
6. Abrams J.H., Barke R.A., Cerra F.B. Quantitative evaluation of clinical course in.surgical ICU patients: The data conform to catastrophe theory //J. Trauma.— 1984 - Vol. 24. № 12.- P. 102S-1037.
7. Anvanzolini G., Barbini P., Gnudi G., Grossi A. Cluster analysis of clinical data measured in the surgical intensive care unit //Comput. Method. Progr. Biomed.— 1991.- Vol. 35. № 3.- P. 157-170.
8. Asher E., Garrison R., Rutcliffe D., Fry D. Endotoxin. cellular function and nutrient blood now//Arch.Surg,-1983.-Vol. 118. № 5.-P. 444-446.
9. Burke J.F. Bondoc Wound sepsis: prevention and control //The management of trauma.— Philadelphia. 1979.— P. 755—766.
10. Cerra F.B., Siegel J.H., Border J.H., Wiles J., McMenamy R.R. The hepatic failure of sepsis: cellular versus substrate //Surgery.—1979.— Vol. 86, № 3. — P. 409-422.
11. Coleman B., Siegel J.H. Statistical treatment of clinical data / Trauma: Emergency surgery & critical care. New York: Edinburgh; London: Melbourne, 1987, P. 97 - 121.
12. Dellinger E.P. Use of scoring systems to assess patients with surgical sepsis //Surg. Clin. North Amer.- 1988.-Vol. 68, № l.-P. 123-145.
13. Edwards J.D. Predicting outcome in sepsis //Crit.Care Med.—1993.— Vol. 21, № 12.- P. 1819-1820.
14. Elebute E.A., Stoner H.B. The grading of sepsis //Brit. J. Surg.— 1983.— Vol. 70. № l.-P. 29-39.
15. Eubans P.J., De Virgilio C., Klein S., Bongurd F. Candida sepsis in surgical patients // Amer. J. Surg.-1993.- Vol. 166, N 6.- P. 617-620.
16. Friedman J.H., Goldwyn P.M., Siegel J.H. The use and interpretation of multivariate methods in the classification of stages of serious infections disease processes in the critically ill //Perspectives in Biometrics.— New-York, 1975.—P. 81—122.
17. Fry D.E., Pearlstein L., Fulton R.L. el al. Multiple system organ failure // Arch.Surg.-19SO.-Vol. 115. № l.-P. 136-140.
IS. Fry D.E. Multiple system organ failure: Pathogenesis and management.— Chicago: Year Book Mod. Publ 1990.- 450 p.
19. Gutierrez G. Summary of the round table conference on tissue oxygen utilization //Intensive Care. Mod. - 1991.- Vol. 17. № l.-P. 67-68.
20. Harkema J.M., Gorman M.W., Bieber L.L. Chaudry I.H. Metabolic interaction between skeletal muscle and liver during hacleriemia //Arch.Surg.—1988.— Vol. 123., № 11.- P. 1415- 1419.
21. Hill M. BMDP User's digest: BMDP Stalislieal Software. Inc. Los Angeles. 1987.-7.5 p.
22. Jeckstadt P., Wittmann D.H. Index fur Beurtcilung der Prognose inlraabdomineiler Infectionem //Fortschr. Antineoplasi. Antimicroh. Chemother.—1983.— Vol. 2. № 4.-P. 517-524.
23. Knaus W.A., Zimmerman J.E., Wagner D.P. et al. APACHE — acute physiology and chronic health evaluation: A physiologically based classification system // Cni.Care Mod.-1981.- Vol. 9, № 5.-P. 591-597.
24. Knaus W.A., Wagner D.P., Draper E.A. The value ol measuring severity of discase in clinical research on acutely ill patients //.I. Chronic. Dis—1984.—Vol. 37, № 3.-P. 455-463.
25. Knaus W.A., Druper E.A., Wagner D.P. et al. APACHE II: A severity of disease classification system //Crit.Care Mcd.— 1985 — Vol. 13. № 7.— P. 818—829.
26. Knaus W.A., Wugner D.P., Zynn J. Short-term mortality predictions for critically ill hospitalized adults: Science and ethics // Science.— 1991.— Vol. 254. № 5030.— P. 389—394.
27. Marzella L.L., Trump B.F. Cell injury and its meaning in shock and resuscitation // Trauma: Emergency surgery & critical care. — New York; Edinburgh; London; Melbourne. 1987.— P. 35 — 56.
28. Meakins J.L., Solonikin J.S., Alio M.D. et al. A proposed classification of intraabdominal infections//Arch. Surg.— 1984.—Vol. 119, № 12.—P. 1372—137S.
29. Nespoli A., Ciara O., Clement M. G. et al. The cardiorespiratory impairment in cirrhosis and sepsis.: An experimental interpretation using octopaminc infusion // Circ.Shock.- 1983.- Vol. 10. № 1.-P15-30.
30. Scirmiento J., Torres A., Guardiolu J.J. et al. Statistical modeling of prognostic indices for evaluation of critically ill patients //Crit.Care.Vied.— 1991.— Vol. 19, №7.- P. 867- 870.
31. Siegel J.H., Goldwyn P.M., Friedman H.P. Pattern and process in the evolution of human septic shock //Surgery.—1971.— Vol. 70, N 2.— P. 232—245.
32. Siegel J. H., Furrell E.J., Goldwyn P.M., Friedman H.P. The surgical implications of physiologic patterns in myocardial infarction shock //Surgery. — 1972.— Vol. 72. №. -P. 126-141.
33. Siegel J.H., Farrell E.J., Miller M. et al. Cardiorespiralory interactions as determinants of survival and the need for respiratory support in human shock slates // J. Trauma. -1973.- Vol. 13. N 7.- P. 602-618.
34. Siegel J.H., Cerra F.B., Colenum B. et al. Physiologic and metabolic correlations in human sepsis //Surgery,— 1979.— Vol. 86. № 2.— P. 163—193.
35. Siegel J.H., Cerra F.B., Peters D. et al. The physiologic recovery trajectory as the organizing principle for the quanlification of hormonometabolic adaptation to surgical stress and severe sepsis. //Adv. Shock Res-1979 — Vol. 2.- P. 177-203.
36. Siegel J.H., Giovannini I., Coleman B. Ventilation: perfusion Maldistribution secondary to the hyperdynamic cardiovascular state as the major cause of increased pulmonary shunting in human sepsis // J.Trauma.— 1979.— Vol. 19. № 6.— P. 432-460.
37. Siegel J.H., Cerra F.B Moody E.A. et at. The effect on survival of critically ill and injured patients of an ICU teaching service organized about a computer-based physiologic CARE system //J.Trauma.- 1980.-Vol. 80. № 7.-P. 558-579.
38. Siegel J.H. Relations between circulatory and metabolic changes in sepsis // Ann.Rev.Mcd.- 1981.- Vol. 32, № 2.- P. 175-194.
39. Siegel J.H., Giovaninni I., Cerra F.B., Nespoli A. Pathologic synergy in cardiovascular and respiratory compensation with cirrhosis and sepsis: A manifestation of a common metabolic deflect'? //Arch.Surg.- 1982.-Vol. 117, № 3.-P. 225-238.
40. Siegel J. H. Cardiorespiratory manifestations of metabolic failure in sepsis and the multiple organ failure syndrome //Surg. Clin. North Amer. —1983.—Vol. 63. № 2, P. 379-399.
41. Siegel J.H., Linberg S.E., Wiles C.E. Therapy of low flow shock states // Trauma: Emergency surgery & critical care.— New York: Edinburgh: London: Melbourne, 1987.- P. 201-287.
42. Siegel J.H., Vary T.C. Sepsis, abnormal metabolic control, and the multiple organ failure syndrome //Trauma: Emergency surgery & critical care.— New York: Edinburgh; Eondon: Melbourne. 1987.— P. 411—503.
43. Skau T., Nystrom P.O., Carlsson C. Severity of illness in intraabdominal infection //Arch. Surg.-1986.- Vol. 121. № 1.-147-152.
44. Stevens L.E. Gauging the severity of surgical sepsis //Arch. Surg.—1983.—Vol. 118, № 10.-P. 1190-1192.
45. Wacka H., Linder M.M., Feldman U. Mannheim peritonitis index: Prediction of risk death from peritonitis: Construction of a statistical and validation of an empirically based index //Theor. Surg.- 1987.- Vol. 1. № 2.- P. 169-177.
46. Weil M.H., Shubin H Biddle M. Shock caused by gram-negative microorganisms: Analysis of 169 cases //Ann. Int. Med.- 1964- Vol. 60. № 3.- P. 384-388.
47. Weil M.H., Ajfi A. Experimental and clinical studies on lactat and piruvate as indicators of the severity of acute circulatory shock //Circulation. — 1970.— Vol. 41, № 6.- P. 989-994.
48. Weisman O. Mediators of inflammation.— New York: London: Plenum Press, 1974.- 205 p.
Глава 5. СИСТЕМНАЯ ВОСПАЛИТЕЛЬНАЯ РЕАКЦИЯ И СЕПСИС У ПОСТРАДАВШИХ С ТЯЖЕЛОЙ МЕХАНИЧЕСКОЙ ТРАВМОЙ
(КАК ПОСЛЕДЕЙСТВИЕ ПЕРЕНЕСЕННОГО ЭКСТРЕМАЛЬНОГО СОСТОЯНИЯ)
“Прямое подтверждение сепсиса. обычно запаздывает, а решает исход быстрое лечение, раннее его начало. Полному диагноз должен ставиться на основании косвенных признаков сепсиса — клинических и лабораторных”.
А.П.Колесов “Госпитальная инфекция”
Главное отличие современного этапа изучения хирургической инфекции состоит в формировании углубленных представлений о механизмах взаимодействия макроорганизма (с его индивидуальными особенностями и системными нарушениями), с одной стороны, и микрофлоры (с ее динамической изменчивостью и сложностью своих. микробиологических, факторов) — с другой. Тяжелая сочетанная травма представляет собой весьма демонстративную клиническую модель. на которой реально прослеживается сложность, многофакторность такого взаимодействия. В результате глубоких системных нарушений после перенесенного экстремального состояния организм утрачивает способность к подавлению инфекционного процесса в зоне повреждения и за ее пределами. Это определяет высокую предуготованность организма к тяжелым формам раневой инфекции, приобретающим выраженную тенденцию к генерализации и развитию сепсиса. Однако клиническое наблюдение способно зафиксировать только уже развивающийся инфекционный процесс. Следовательно, задача состоит в том. чтобы, оценивая функциональный ущерб, обусловленный перенесенным экстремальным состоянием, выделить некоторые специфические изменения, позволяющие заблаговременно распознать уже развивающуюся генерализацию инфекционного процесса.
Следует заметить, что специфика изменений, определяющих готовность поврежденного организма к вступлению в инфекционный процесс, изначально приобретающий тенденцию к генерализации. не получает полного отражения в динамике показателей иммунитета. Известно, что на ранних этапах развития травматической болезни ей всегда сопутствует временный вторичный иммунодефицит, выраженность которого далеко не всегда позволяет достоверно прогнозировать развитие раневой инфекции и ее тяжесть. Не решают задачу также хорошо известные признаки общей реакции организма на очаг воспаления, которые соотносятся с особенностями течения уже существующего местного инфекционно-воспалительного процесса. Наиболее полно смысл посттравматических изменений, характеризующих готовность организма к развитию генерализованных форм раневой инфекции, обозначается понятием синдрома системной воспалительной реакции.
Введение в клиническую практику в 1991 году понятия о синдроме системной воспалительной реакции было рекомендовано на совместной конференции реаниматологов и пульмонологов США. Канады и ряда других стран [13—15). Следует подчеркнуть некоторую условность терминологии. Речь идет не о постулировании общеизвестных классических признаков локального воспалительного процесса, а о выделении специфического типа реакции организма на повреждающее воздействие, который, имея в своей основе воспалительную реакцию, принимает уже генерализованный, патологический характер. Решениями конференции были рекомендованы следующие критерии диагностики синдрома системной воспалительной реакции:
— Температура выше 38 °С или ниже 36 °С;
— Частота сердечных сокращений свыше 90 уд/мин;
— Частота дыхательных движений свыше 20 в минуту или Расо2 меньше 32 мм рт.ст.;
— Количество лейкоцитов выше 72 • 109 к/л, ниже 4 • 109 к/л или число незрелых форм превышает 10 %.
В соответствии с принятыми документами, предлагается диагностику синдрома системной воспалительной реакции осуществлять при наличии как минимум двух из перечисленных четырех признаков. Сепсис считается диагностированным (как было зафиксировано в решениях конференции) при наличии документально подтвержденной инфекции и положительных признаков (как минимум двух) синдрома системной воспалительной реакции.
Однако такой подход оставляет место для некоторых методологических неточностей, относящихся прежде всего к диагностике синдрома системной воспалительной реакции у такой крайне тяжелой категории больных, как пострадавшие с тяжелой механической травмой.
Нам представляется, что у данной категории больных о синдроме системной воспалительной реакции как о патологическом процессе допустимо говорить лишь при обязательном присутствии всех указанных диагностических критериев. Это позволит выделить наиболее тяжелый контингент пострадавших с генерализованными воспалительными процессами, что. несомненно, будет способствовать дальнейшему углублению наших представлений об этой патологии.
В таком случае посттравматический (или раневой) сепсис может быть определен как генерализованная форма хирургической инфекции, развивающаяся на фоне синдрома системной воспалительной реакции при доказанной циркуляции возбудителя (бактерии, вирусы и другие микроорганизмы) в кровеносном русле.
Следует заметить, что данное определение ни в коей мере не противоречит сложившемуся более общему определению сепсиса как патологического процесса, характеризующегося утратой возможности подавления вегетации возбудителя за пределами инфекционного очага. Оно лишь устанавливает конкретную связь такой утраты с системной воспалительной реакцией.
Иными словами, синдром системной воспалительной реакции может развиться в ответ на тяжелое механическое повреждение, осложненное или неосложненное инфекционным процессом в ране. При этом развитие синдрома системной воспалительной реакции (ССВР) при доказанной циркуляции в крови патогенного возбудителя следует расценивать как сепсис.
Такое толкование сепсиса только на первый взгляд представляется новым. На самом же деле оно лишь позволяет с большей определенностью сформулировать конкретное понимание патогенетической сущности этого грозного осложнения тяжелой механической травмы и детализировать принципы его диагностики. Следует подчеркнуть, что представленное определение сепсиса не входит в смысловое противоречие с прежними, ставшими классическими, определениями В.Я.Шлапоберского (1952). И.В.Давыдовского, (1944). Б.М.Костюченка (1982), В.Г.Бочоришвили (1988) [1, 5. 12] и др. Оно является, на наш взгляд, конструктивным их дополнением и исключает двусмысленность толкования этого процесса, устраняя, такое понятие, как “сепсис без возбудителя”. только вызывающее терминологическую путаницу.
Предыдущая глава посвящена методологии разработки системы функционального компьютерного мониторинга в распознавании узловых клинико-патогенетических параллелей синдрома системной воспалительной реакции в раннем постшоковом периоде. Исходя из этого сформулирован и обоснован общий подход к использованию системы функционального компьютерного мониторинга (СФКМ) в клинике. Главная цель настоящей главы состоит в том. чтобы выделить типичные формы течения постшокового периода на основе изучения клинических признаков системной воспалительной реакции в сопоставлении с критериями функционального компьютерного мониторинга.
В ходе проведения комплексных сравнительных исследований динамики раннею иостшокового периода у пострадавших с механической травмой, использования данных клинического наблюдения, лабораторных показателей и критериев системы функционального компьютерного мониторинга удалось выделить четыре различных типа его течения.
Здесь необходимо еще раз подчеркнуть, что разделение неосложненного и осложненного течения травматической болезни преднамеренно рассматривалось нами только применительно к развитию синдрома системной воспалительной реакции (ССВР).
Однако в ходе исследования стало ясно. что наличие ССВР знаменует тяжелое, рефрактерное течение травматической болезни и ее осложнений с высокой угрозой развития сепсиса и неблагоприятного исхода. Поэтому разграничение осложненного и неосложненного течения ориентировано не только на идентификацию синдрома системной воспалительной реакции, но имеет более глубокий прогностический смысл.
Прежде всего это неосложненное течение. Оно характеризуется отсутствием каких-либо клинических признаков осложнений, отмечается положительная динамика всех лабораторных показателей и критериев системы функционального компьютерного мониторинга (ФКМ).
В результате сопоставления клинических, лабораторных данных и критериев системы функционального компьютерного мониторинга удалось выделить промежуточный тип между неосложненным течением и развитием клиники синдрома системной воспалительной реакции. получивший название “состояние, “угрожающее” развитием синдрома системной воспалительной реакции”.
Пострадавшие с имеющимися признаками ССВР, но без бактериемии, были отнесены в третью группу. Отдельно проанализированы наблюдения у пострадавших с диагностированным сепсисом.
 2015-05-06
2015-05-06 365
365








