С точки зрения возможности противостояния организма новорожденных инфицированию, в биологическом плане важное значение имеет грудное вскармливание ребенка. В молочных железах матери происходит секреция иммуноглобулинов из сыворотки крови, а также локальный биосинтез антител, поэтому грудное молоко играет важную роль в обеспечении иммунологической защиты новорожденного. В первые 5 суток лактации секретируется молозиво, затем — транзиторное, или промежуточное, молоко, начиная с 15-го дня образуется зрелое молоко. Молозиво и молоко содержат все классы сывороточных иммуноглобулинов и секреторный IgA. Кроме того, в молоке содержатся белки системы комплемента, лактоферрин, лизоцим, цитокины (интерфероны и
интерлейкины), выявляются практически все типы иммунокомпетентных клеток — макрофаги, Т- и В-лимфоциты, а также жизнеспособные нейтрофилы и другие лейкоциты.
Клинические наблюдения указывают на положительную роль грудного молока для создания и поддержания пассивного естественного иммунитета в основных биотопах (желудочно-кишечном, бронхолегочном и урогенитальном) организма новорожденного. Вследствие этого, вскармливание детей грудью существенно снижает частоту кишечных и респираторных инфекций.
Содержание иммуноглобулинов А класса в молозиве женщин существенно выше, чем других классов. Более 90 % из них составляет секреторный иммуноглобулин А. Нейтрофилы, моноциты и макрофаги способны к фагоцитозу и умерщвлению бактерий, грибов, а также проявлению антителозависимой цитотоксичности. Макрофаги содержат внутриклеточно и продуцируют лизоцим, лактоферрин, компоненты комплемента, цитокины. В молоке содержатся эффекторные и регуляторные Т-лимфоциты, Т-клетки памяти. Все это облегчает возможность иммунной системы новорожденного отвечать на различные вирусные и бактериальные антигены. Эти клетки и продукты их активации стимулируют В-лимфоциты к биосинтезу специфических иммуноглобулинов А.
Молекулы и клетки иммунной системы матери, содержащиеся в молоке, восполняют незрелость иммунной системы новорожденного. Эта компенсация достигается поступлением антигенспецифических антител в желудочно-кишечный тракт новорожденного, а затем в респираторный тракт и другие области организма.
Грудное молоко содержит также огромное число неспецифических протективных факторов с разным механизмом антимикробного действия:
- полисахариды и гликопротеиды, предотвращающие адгезию патогенов (ротавирусы, ВИЧ, кишечная палочка, пневмококк, кампилобактер) к эпителию слизистой;
- лактоферрин (полипептид из 18 аминокислот), обладающий бактерицидной активностью;
- К-казеин, ингибирующий адгезию хеликобактера;
- лизоцим, обладающий бактериостатическим эффектом;
- жирные кислоты и моноглицериды, оказывающие литический эффект в отношении простейших, вирусов и бактерий;
- гормоны и ростовые факторы молока, способствующие созреванию желудочно-кишечного и респираторного тракта, снижают потенциальную инвазивность широко распространенных патогенов.
Установлена обратная зависимость между концентрацией в грудном молоке секреторного иммуноглобулина А и частотой высеваемости кишечной палочки из фекалий новорожденных. Секреторные антитела — IgA — грудного молока взаимодействуют с пневмококками, стрептококками, энтеровирусами, а также нейтрализуют эндо- и экзотоксины грамотрицательных бактерий.
КРИТИЧЕСКИЕ ПЕРИОДЫ РАЗВИТИЯ ИММУННОЙ СИСТЕМЫ
ДЕТСКОГО ОРГАНИЗМА
Критический период — этап развития и функционирования детского организма, характеризующийся наиболее низким уровнем защищенности, неэффективностью функции иммунной системы, необычайно высокой восприимчивостью к инфекции и сопряженный с нейрогуморальными, структурно-функциональными и/или геномическими перестройками организма в соответствии с возрастной стратегией развития. Отражением физиологических процессов развития иммунной системы детского организма является перестройка
миело- и лимфопоэза (рис. 3) в разные возрастные периоды жизни.
|

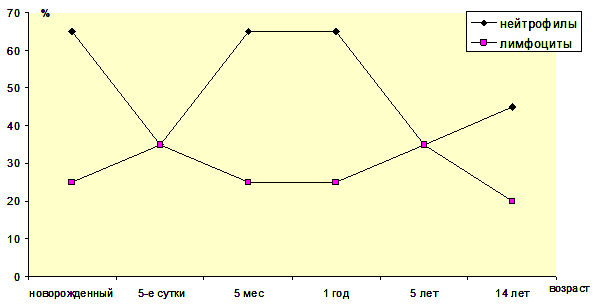
Рис. 3. Физиологические процессы миело- и лимфопоэза в разные возрастные
периоды развития детского организма
В период внутриутробного развития критическими считаются 8–12-я недели — время закладки основных структур иммунной системы, отлаживания механизмов дифференцировки клеток и органов иммунной системы плода.
В постнатальном развитии иммунной системы ребенка выделяют несколько таких периодов.
Первый период ассоциирован с новорожденностью и длится в среднем 25–35 дней. В это время отмечаются существенные изменения лейкоцитарной формулы: снижение количества клеток гранулоцитарного ряда и повышение лимфоцитарного пула клеток (абсолютный лимфоцитоз). При этом организм ребенка впервые подвергается атаке ранее незнакомых для иммунной системы многочисленных эндо- и экзогенных патогенов и их антигенов. Гуморальный и клеточный иммунитет, неспецифические факторы видового иммунитета в это время еще незрелы и малоэффективны. Пассивный материнский иммунитет варьирует и также относителен (у значительной части новорожденных материнские антитела отсутствуют или находятся на невысоком уровне). Именно в этот период отмечается наибольшая восприимчивость детей к патогенным и условно-патогенным микроорганизмам с развитием локальных (гнойно-воспалительных, респираторных, кишечных) и системных (бактериемия, сепсис) инфекций.
Второй период формируется между 3-м и 6-м месяцами жизни ребенка. Он обусловлен двумя факторами: а) постепенным ослаблением и исчезновением пассивного специфического материнского иммунитета; б) отставанием морфофункционального созревания иммунной системы некоторых детей. Этот период характеризуется слабыми возможностями для развития собственного гуморального и клеточного иммунного ответа, непродолжительной иммунологической памятью, развитием ненапряженного противоинфекционного активного естественного и искусственного иммунитета. При этом преимущественно формируется первичный иммунный ответ с синтезом низкоаффинных полиспецифических антител — IgM. Местный иммунитет также ослаблен. Для развития вторичного протективного иммунного ответа на детские вакцины против дифтерии, столбняка, коклюша, полиомиелита, кори требуется трехкратная иммунизация. Незрелость иммунной системы проявляется обычно повышенной чувствительностью таких детей к респираторным вирусным инфекциям (аденовирусам, вирусам гриппа и парагриппа, РСВ). К этому периоду среди новорожденных уже выявляются дети, характеризующиеся относительно более частым возникновением и длительным течением инфекций. Это своеобразный индикатор того, что у некоторых из них могут иметься определенные типы первичных генетических дефектов иммунной системы (преимущественно В-зависимых).
Синдром внезапной смерти. Особенностью перестройки иммунной системы детей этого периода является спонтанное возникновение у них синдрома внезапной смерти. Этот синдром является ведущей причиной летальности детей постнатального периода в развитых странах. Пик летальности приходится на возрастной промежуток между 1-й неделей и 1-м годом (наиболее часто возникает между 2-й неделей и 4-м месяцем) после рождения. Большинство случаев смерти приходится на зимний период. Синдром, как правило, возникает у детей с респираторной патологией, родившихся от курящих матерей. Смерть наступает внезапно во время сна в положении ничком. Возможные причины синдрома интенсивно исследуются. Предположительно этиологическими факторами являются измененная иммунологическая реактивность, инфекционные агенты респираторного тракта и их токсины. К инфекционным агентам, способствующим высокому риску развития синдрома внезапной смерти, относят возбудителей респираторной патологии преимущественно бактериальной природы: стафилококки, бордетеллы, Haemophilus influenzae, клостридии, кишечную палочку, хеликобактер и их токсины. Особую роль в генезе синдрома отводят экзотоксинам данных микроорганизмов, являющихся суперантигенами, вызывающими гиперстимуляцию Т-системы лимфоцитов, избыточную продукцию цитокинов. Гипрепродукция цитокинов IL-1, IL-6, TNF, а также высокий уровень IgE и повышенная функция Tх2 типа в связи с этим синдромом интенсивно обсуждаются.
Третий период проявляется на 2-м году жизни ребенка. На это время приходится важный физиологический переход формирования адаптивного иммунитета — созревание способности переключения изотипов иммуноглобулинов с IgM на IgG (вначале приобретается возможность синтеза IgG1, IgG3, а затем IgG2 и IgG4). В целом, системный и особенно местный иммунитет еще остаются недостаточно эффективными, сохраняется высокая восприимчивость к инфекциям. Это связано с недостаточностью регуляторной функции CD4+Tх1 типа, продукцией ИФН-g, взаимодействия CD4+ Tх2 типа с В-лимфоцитами.
Четвертый период проявляется между 4-м и 6-м годами развития ребенка и связан со второй перестройкой в кроветворении и с изменением содержания основных типов форменных элементов. Следует отметить, что к этому возрасту у большинства детей иммунологические параметры уже близки к уровню взрослых. Иммунная система ребенка уже имеет достаточный персональный опыт по организации специфической противоинфекционной защиты от естественной локальной и системной инфекций, а также иммунного ответа на вакцинные препараты. К этому времени в популяции достаточно четко формируется группа часто и длительно болеющих респираторной патологией детей (ЧДБ). Частота респираторных инфекций в течение года может достигать 6–10 раз. Особенностью иммунной системы таких детей является сниженный уровень секреторного иммуноглобулина А или его селективный дефицит. У значительной части детей при этом отмечается повышение биосинтеза иммуноглобулинов Е, что является свидетельством доминирования функции CD4+ T-клеток Tх2 типа над субпопуляцией Tх1 типа. Для таких детей характерно более частое развитие атопических, паразитарных и иммунокомплексных процессов.
Пятый период в формировании иммунной системы ребенка приходится на подростковый возраст и обусловлен половой дифференциацией и процессами созревания организма. Начинается в возрасте 13–14 лет у мальчиков и 11–13 лет у девочек. Половые гормоны — андрогены и эстрогены — воздействуют на органы и клетки-мишени иммунной системы, стимулируют или ингибируют определенные субпопуляции, регуляторные и эффекторные механизмы. При этом отмечается снижение массы лимфоидных органов. Под действием андрогенов происходит подавление клеточного и стимуляция гуморального звена иммунитета. В этот период возможно формирование ряда иммунопатологических процессов, которые впоследствии могут способствовать формированию определенных иммунопатологических заболеваний. Базируются они на основе некоторых первичных или развившихся к этому времени вторичных иммунодефицитных состояний.
СИСТЕМА «МАТЬ–ПЛОД». ИММУНологическиЕ
ВЗАИМООТНОШЕНИЯ МАТЕРИ И ПЛОДА
Основная особенность беременности заключается в том, что плод по отношению к матери является генетически наполовину чужеродным организмом, который до положенного срока не отторгается. Аллогенность (чужеродность) плода заключается в том, что все клетки содержат гаплоидный набор ГКГС-антигенов не только матери, но и отца.
Особую опасность для клеток плода представляет иммунный ответ матери с развитием клонов Т-киллерных клеток (CD8+), специфичных к отцовским антигенам ГКГС I и II классов, ЕКК (CD16+ клетки) и цитотоксических антител против отцовских антигенов.
 Поэтому с первых часов после зачатия и до момента родов развиваются супрессорные механизмы, которые не позволяют иммунной системе матери осуществлять атаку на плод и вызывать его отторжение на всех этапах развития.
Поэтому с первых часов после зачатия и до момента родов развиваются супрессорные механизмы, которые не позволяют иммунной системе матери осуществлять атаку на плод и вызывать его отторжение на всех этапах развития.
Роль иммуносупрессии в иммунологических реакциях «мать–плод» описана впервые в 1953 году. Стало классикой говорить о «состоянии иммунотолерантности матери к своему плоду». Результаты научных работ последних лет существенно расширили понимание этой проблемы.
Развивающаяся супрессия многофакторна и формируется за счет изменений в системных (особенность функционирования иммунной системы матери в период беременности) и местных иммунных реакциях (функционирование фетоплацентарной единицы).
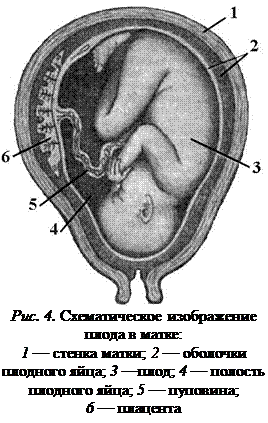
Во время беременности особую важность приобретает фетоплацентарная единица, которая индуцирует изменения в гормональном спектре матери и отвечает за динамическую перестройку иммунной системы (рис. 4).
 2015-05-06
2015-05-06 1097
1097








