1. Напишите кинетические уравнения для скоростей следующих реакций:
а) 2СО(г.) + CI2(г.) → 2СОCI 2(г.) б) С(тв.)+ СО2(г.) → 2СО(г.)
в) СаО(тв)+ СО2(г.) →СаСО3(тв) г) 4NН3 (г) + 3О2 (г) ® 2N2 (г) + 6Н2О(г)
Какие из вышеперечисленных реакций относятся к гомогенным, какие – к гетерогенным?
2. Как изменится скорость реакции
2NO (г) + O2(г) → 2 NO2(г), если:
а) увеличить давление в системе в 2 раза, б) повысить концентрацию NO в 2 раза, в) повысить концентрацию О2 в 2 раза?
3. Температурный коэффициент реакции равен 3. Во сколько раз увеличится скорость реакции при увеличении температуры на 400?
4. При увеличении температуры на 800, скорость реакции возросла в 256 раз. Рассчитайте значение температурного коэффициента скорости реакции.
5. В каком направлении сместится равновесие следующих реакций
2 СО(г) + О2 (г) 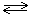 2 СО2 (г) Δ Н < 0
2 СО2 (г) Δ Н < 0
СаСО3 (тв) 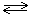 СаО(тв) + СО Δ Н > 0
СаО(тв) + СО Δ Н > 0
N2(г) + 3H2(г) 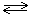 2 NH3(г) Δ H < 0
2 NH3(г) Δ H < 0
2Mg + O2(г) 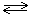 2MgO Δ H < 0
2MgO Δ H < 0
а) при понижении температуры?
б) при повышении давления?
 2015-05-10
2015-05-10 933
933








