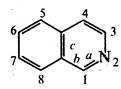
 Ізохінолін (бензо[ с ]піридин) є ізомером хіноліну. Молекула ізохіноліну, як і хіноліну, складається з конденсованих піридинового та бензольного циклів, але, на відміну від хіноліну, цикли з'єднані вздовж зв'язку С3-С4 піридинового кільця. Нумерацію атомів ізохінолінового ядра проводять згідно з правилами ІЮПАК наведеним способом.
Ізохінолін (бензо[ с ]піридин) є ізомером хіноліну. Молекула ізохіноліну, як і хіноліну, складається з конденсованих піридинового та бензольного циклів, але, на відміну від хіноліну, цикли з'єднані вздовж зв'язку С3-С4 піридинового кільця. Нумерацію атомів ізохінолінового ядра проводять згідно з правилами ІЮПАК наведеним способом.
А. Способи добування
Ізохінолін міститься в хіноліновій фракції кам'яновугільної смоли (близько 1%), з якої його здобувають у вигляді солі (гідросульфату).
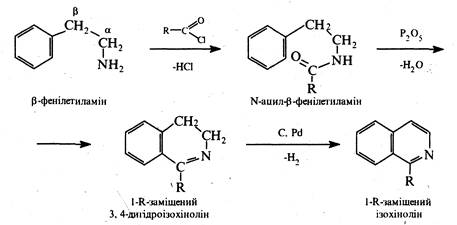
Одним з поширених способів синтезу ізохіноліну та його похідних є реакція Бішлера-Напіральського (1893 p.), котра ґрунтується на циклізації N-ацильних похідних β-фенілетил амінів у 3,4-дигідроізо-хіноліни та дальшому перетворенні останніх на ізохіноліни шляхом каталітичного дегідрування над паладієм на вугіллі. Циклізацію N-ацильних похідних здійснюють частіше в присутності Р2О5 або РОС13 в ксилолі.
Б. Фізичні властивості
Ізохінолін безбарвна кристалічна речовина (т. пл. 24,6 °С), розчинна у воді, етанолі, діетиловому ефірі, хлороформі та бензолі.
За хімічними властивостями ізохінолін мало чим відрізняється від хіноліну. За рахунок гетероатома він виявляє оснбвні властивості та легко утворює солі з кислотами, алкіл- і ацилгалогенідами. Як основа ізохінолін трохи сильніше хіноліну (рКВН+ ізохіноліну 5,14; рКВН+ хіноліну 4,94).
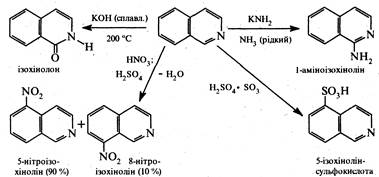
Реакції електрофільного заміщення, як і в ядрі хіноліну, проходять здебільшого в положеннях 5 і 8. Нуклеофільне заміщення в ізохіноліновому циклі відбувається переважно у положенні 1.
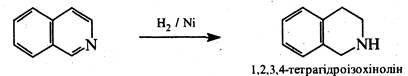
При відновленні ізохіноліну, як і у молекулі хіноліну, в першу чергу гідрується піридинове ядро. Так, при дії натрієм в етанолі або воднем над нікелевим каталізатором ізохінолін відновлюється до 1,2,3,4-тетрагідроізохіноліну.
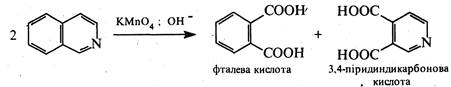
За жорсткіших умов гідруванню піддається і бензольне кільце. При окисненні ізохіноліну лужним розчином КМnО4 утворюється суміш фталевої та 3,4-піридиндикарбонової кислот:
Під дією органічних пероксикислот ізохінолін окиснюється по гетероатому, утворюючи N-оксид.
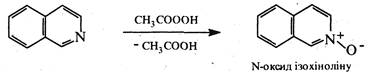
 2015-07-14
2015-07-14 2585
2585








