Акумуляторні батареї (були одним з перших комерційних продуктів, заснованих на застосовуваннях полімерних сполук, що проводять. У якості матеріалу позитивного електроду в них використовують поліпірол, политіофен або поліанілін. Матеріалом для виготовлення негативних електродів зазвичай служать літій або його сплави (наприклад, з алюмінієм).
В процесі розряду акумулятора електрони рухаються від негативного електроду до позитивного по зовнішньому ланцюгу. При цьому літій окислюється, переходячи в електроліт у вигляді позитивно заряджених іонів, полімерне з'єднання відновлюється, що супроводжується переходом заряд компенсованих аніонів з полімеру в електроліт. При заряді акумулятора від зовнішнього джерела струму на електродах протікають зворотні процеси.
Електролітом може бути як сольовий розчин на основі пропіленкарбонату, що часто використовується як розчинник в джерелах струму, так і полімерна мембрана, насичена відповідною сіллю літію (твердий полімерний електроліт). У останньому випадку акумулятор зовсім не містить рідкої фази, що робить його найбільш безпечним і зручним [12].
На сьогодні розроблено вже декілька поколінь суперконденсаторів (СК), а саме на основі вуглецевих матеріалів, оксидів металів та електроактивних полімерів. У першому типі СК джерело накопичення енергії є справді електростатичним. Електродами у цьому випадку є ідентичні пористі вуглецеві електроди з високорозвинутою питомою поверхнею (симетричний СК) і ємність виникає в результаті розділення заряду на межі тверда поверхня|рідкий електроліт. Здебільшого ємність ПЕШ на поверхні вуглецю та металів становить 10-40 мкФ·см-2, а питома ємність високо розвинутої вуглецевої поверхні - ~4 Ф·кг-1. Енергію W та потужність Р для такого типу суперконденсаторів можна розрахувати за формулами:
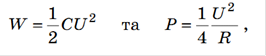
МЕТОДИКА ЕКСПЕРИМЕНТАЛЬНОГО ДОСЛІДЖЕННЯ
Опис вихідних речовин
Під час синтезу композитів, а також одержання композитів на основі поліпіролу та поліаніліну використовували наступні речовини та матеріали:
MоO3;
ванадат амонія (NH4VO3);
дистильована вода;
сульфатна кислота (H2SO4);
ППірол;
ПАн;
графіт.
Фізико-хімічна характеристика досліджуваних речовин
2 - порошок жовтого кольору, розчинний у воді. Мr = 143,94 г/моль; Тпл.= 795 °С; Ткип.= 1255 °С Найбільш стійкі сполуки молібдену, широко поширені в земній корі (молібденіт (MoS2)).ЛД= 125мг/кг.
Пірол - розчинний у воді; змішується з органічними розчинниками. Полімеризується під дією кислот. Tкип.=129,76ºС, Тпл = -23,42ºС.
NH4VO3 - білі або жовтуваті кристали, розчинні у воді. Тпл =138 ºС.
Анілі́н - (C6H5NH2), найпростіший ароматичний амін. Безбарвна рідина, малорозчинна у воді, змішується з спиртом, ефіром, бензолом; Під впливом повітря швидко темніє, стає коричневою. Пара його отруйна. t° кип. 184,4С°, t° плав. - 6°С.
 2020-04-20
2020-04-20 197
197








