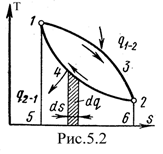
 Энтропию можно применять совместно с одним из основных параметров для графического изображения процессов. Удобнее всего энтропию сочетать с абсолютной температурой Т. Если энтропию s откладывать по оси абсцисс, а абсолютную температуру—по оси ординат, то получаем координатную систему: Тs, т.е. Ts-диаграмму, где состояние газа графически изобразится точкой, а процесс — в виде кривой, уравнение которой можно представить как Т = f(s). Элементарная теплота процесса dq= Тds изобразится на диаграмме элементарной площадкой, высота которой равна Т, а основание ds (рис. 5.2). Поскольку количество тепла, подводимого в этом процессе
Энтропию можно применять совместно с одним из основных параметров для графического изображения процессов. Удобнее всего энтропию сочетать с абсолютной температурой Т. Если энтропию s откладывать по оси абсцисс, а абсолютную температуру—по оси ординат, то получаем координатную систему: Тs, т.е. Ts-диаграмму, где состояние газа графически изобразится точкой, а процесс — в виде кривой, уравнение которой можно представить как Т = f(s). Элементарная теплота процесса dq= Тds изобразится на диаграмме элементарной площадкой, высота которой равна Т, а основание ds (рис. 5.2). Поскольку количество тепла, подводимого в этом процессе
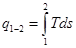 , (5.26)
, (5.26)
то на Тs-диаграмме площадь 1234, ограниченная линией процесса, крайними ординатами и осью s, в некотором масштабе изображает теплоту, участвующую в процессе.
Из уравнения dq = Тds следует, что dq и ds имеют одинаковые знаки. Если в процессе энтропия s увеличивается, то теплота к газу подводится. Если энтропия s уменьшается, то это указывает на отвод теплоты от рабочего тела.
Для идеальных газов условно принято считать энтропию равной нулю при нормальных физических условиях.
ИДЕАЛЬНЫХ ГАЗОВ
Первый закон термодинамики устанавливает взаимосвязь между количеством теплоты, изменением внутренней энергии и внешней работой газа, причем количество теплоты, подводимое к телу или отводимое от него, зависит от характера процесса.
К основным процессам, имеющим большое значение, как для теоретических исследований, так и для практических работ в технике, относятся: изохорный, протекающий при постоянном объеме; изобарный, протекающий при постоянном давлении; изотермный, протекающий при постоянной температуре; адиабатный, протекающий при отсутствии теплообмена с внешней средой.
Кроме того, существует группа процессов, являющихся при определенных условиях обобщающими для основных процессов. Эти процессы называются политропными и характеризуются постоянством теплоемкости в процессе.
Изохорный процесс
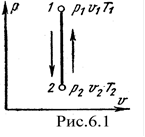
Процесс, протекающий при постоянном объеме, называют изохорным (dυ = 0, или υ = const). Кривая процесса называется изохорой. На рис. 6.1 представлен график процесса.
 Согласно закону Шарля, при постоянном объеме давление газа изменяется прямо пропорционально абсолютным температурам:
Согласно закону Шарля, при постоянном объеме давление газа изменяется прямо пропорционально абсолютным температурам:
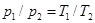 . (6.1)
. (6.1)
Внешняя работа газа при υ=const равна нулю, так как dυ = 0, т.е. l=0.
Основное уравнение первого закона термодинамики (4.6) при d l = 0 принимает вид
dqυ = duυ = cυdt.
Количество теплоты, участвующее в процессе при постоянной теплоемкости, равно
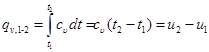 . (6.2)
. (6.2)
Вся внешняя теплота расходуется только на изменение внутренней энергии тела.
Если процесс 1-2, осуществляется с увеличением давления, теплота в нём подводится, при этом увеличивается внутренняя энергия и температура. Если давление газа в процессе понижается, то теплота отводится, уменьшается внутренняя энергия и температура (рис.6.1)
Изменение энтропии в изохорном процессе определяем из уравнения (5.21):
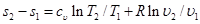 ,
,
но при υ=const ln υ2/υ1=0, поэтому изменение энтропии при постоянной теплоемкости равно
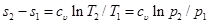 . (6.3)
. (6.3)
Как видно из данного уравнения, изохора на Тs-диаграмме представляет собой логарифмическую кривую.
Изобарный процесс
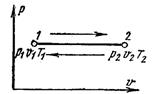
Рис. 6.2
Процесс, протекающий при постоянном давлении, называют изобарным (dр = 0, или р = const). Кривая процесса называется изобарой. На рис. 6.2 изображен график процесса.
Из уравнения состояния идеального газа для изобарного процесса находим
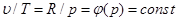
В соответствии с з аконом Гей-Люссака, в изобарном процессе объемы одного и того же количества газа изменяются прямо пропорционально абсолютным температурам:
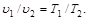 (6.4)
(6.4)
При расширении газа его температура возрастает, при сжатии — уменьшается.
Удельная работа изменения объема при этом выражается следующим уравнением:
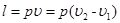 , (6.5)
, (6.5)
или
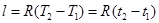 . (6.6)
. (6.6)
Основное уравнение первого закона термодинамики при р=const (dр=0) имеет вид
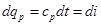 .
.
Следовательно, количество теплоты, сообщенное телу в изобарном процессе при постоянной теплоемкости, равно
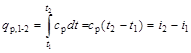 ; (6.7)
; (6.7)
при переменной теплоемкости
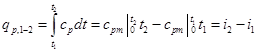 . (6.8)
. (6.8)
Для обратимого изобарного процесса при постоянной теплоемкости изменение энтропии находится по уравнению (5.23):
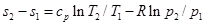 ,
,
но при р = const lnp2/p1=0, поэтому
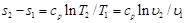 . (6.9)
. (6.9)
Изобара на Тs-диаграмме также, как и изохора, изображается логарифмической кривой.
Площадь под изобарой в некотором масштабе изображает количество теплоты qр, сообщаемое газу, равное изменению энтальпии i 2- i 1.
Из сопоставления уравнений (6.3) и (6.9) следует, что в случае осуществления изохорного и изобарного процессов в одном интервале температур возрастание энтропии будет больше в изобарном процессе, так как ср всегда больше сυ. Изобары являются более пологими кривыми, чем изохоры (см. рис. 6.3).
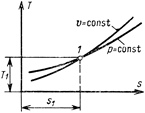
Рис. 6.3
Изотермный процесс
Процесс, протекающий при постоянной температуре, называют изотермным (Т = const, или dТ = 0). Кривая процесса называется изотермой (рис. 6.4).
Для изотермного процесса 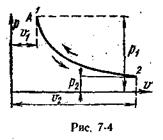 объем газа изменяется обратно пропорционально его давлению (закон Бойля — Мариотта):
объем газа изменяется обратно пропорционально его давлению (закон Бойля — Мариотта):
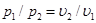 . (6.10)
. (6.10)
На рυ-диаграмме изотермный процесс представляет собой равнобокую гиперболу.
|
dq=d l и q1-2= l 1-2.
Количество подведенной к идеальному газу теплоты численно равно работе изменения объема.
Зная уравнение изотермного процесса для идеального газа, и применяя уравнение состояния, определим удельную работу газа.
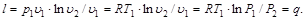 (6.11)
(6.11)
Энтальпия и внутренняя энергия идеального газа не меняются,
т. е. d i =0 и du = 0.
Изотермный процесс на Ts-диаграмме изображается горизонтальной прямой, параллельной оси абсцисс. Для определения изменения энтропии следует воспользоваться уравнениями (5.21) и (5.23) при T=const, после чего плучаем:
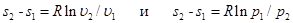 . (6.12)
. (6.12)
Теплота, участвующая в изотермном процессе, равна произведению изменения энтропии (s2 – s1) на абсолютную температуру Т:
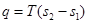 . (6.13)
. (6.13)
Адиабатный процесс
Процесс, протекающий без подвода и отвода теплоты, т. е. при отсутствии теплообмена рабочего тела с окружающей средой, называют адиабатным, а кривая этого процесса называется адиабатой. Для получения адиабатного процесса необходимым и обязательным условием является dq = 0 и, следовательно, q= 0.
Обратимый адиабатный процесс можно осуществить в цилиндре с абсолютно нетеплопроводными стенками при бесконечно медленном перемещении поршня.
Уравнение адиабаты выводится на основе уравнения первого закона термодинамики и имеет вид:
pυk=const. (6.14)
При адиабатном процессе произведение давления на объем газа в степени k есть величина постоянная. Величину k называют показателем адиабаты. Показатель адиабаты k=cp/cυ (см. раздел5.5).
В соответствии с уравнением (6.14) адиабата в pυ – диаграмме графически изображена неравнобокой гиперболой АВ (см. рис. 6.5, а).
Рассмотрим зависимость между основными параметрами в адиабатном процессе.
Из уравнения адиабаты следует, что
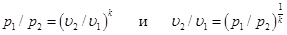 . (6.15)
. (6.15)
Зависимость между температурой, объёмом и давлением газа в процессе выражается соотношением:
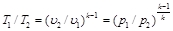 . (6.16)
. (6.16)
Уравнение первого закона термодинамики для адиабатного процесса принимает вид:
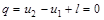
или
l = u1 – u2. (6.17)
Это значит, что работа изменения объема в адиабатном процессе получается за счет убыли внутренней энергии тела;
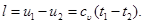 (6.18)
(6.18)
Если газ расширяется, то его внутренняя энергия и температура убывают; если газ сжимается, то его внутренняя энергия и температура возрастают.
Работу газа также можно определить из следующих соотношений:
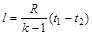 (6.19)
(6.19)
или
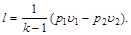 (6.20)
(6.20)
Графически внешняя работа изображается на рυ-диаграмме пл. 12v2v1 (рис. 6.5, а).
Из рис. 6.5 видно, что поскольку в уравнении адиабаты k > 1, она на рυ-диаграмме идет круче, чем изотерма.
Для обратимого адиабатного процесса dq =0, поэтому
ds = dq/T = 0 и s2-s1 = const,
т. е. обратимый адиабатный процесс является одновременно изоэнтропным (или при постоянной энтропии) и изображается в Тs-диаграмме вертикальной прямой 1 – 2, параллельной оси ординат (см. рис. 6.5, б).
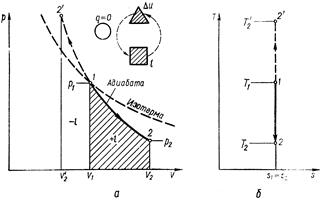
Рис. 6.5
Политропные процессы
Условились всякий процесс идеального газа, в котором теплоемкость является постоянной величиной, называть политропным процессом, а линию процесса — политропой.
Из определения политропного процесса следует, что основные термодинамические процессы — изохорный, изобарный, изотермический и адиабатный, если они протекают при постоянной теплоемкости, являются частными случаями политропного процесса.
Теплоемкость политропного процесса сn может принимать самые разнообразные положительные и отрицательные значения от + ∞ до - ∞.
В результате преобразования аналитических выражений первого закона термодинамики получаем выражение:
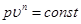 . (6.21)
. (6.21)
Полученное уравнение является уравнением политропного процесса.
Величина n в уравнении (6.21) называется показателем политропы; он равен
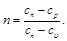 (6.22)
(6.22)
Показатель политропы n принимает для каждого процесса определенное числовое значение. Для основных процессов: изохорных n=±∞, изобарных n = 0, изотермных n = 1 и адиабатных n = k.
Поскольку уравнение политропы отличается от уравнения адиабаты только величиной показателя n, то, очевидно, все соотношения между основными параметрами могут быть представлены формулами, аналогичными адиабатному процессу:
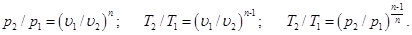
Теплоемкость политропного процесса определяем из формулы
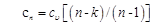 . (6.23)
. (6.23)
Уравнение (6.23) позволяет определить теплоемкость политропного процесса для каждого значения n.
Если в уравнение (6.23) подставить значения n для частных случаев, то получаем теплоемкости рассмотренных процессов:
изохорного процесса n=±∞, cn=сυ;
изобарного процесса n=0, cn=kсυ=cp;
изотермного процесса n=1, cn=±∞;
адиабатного процесса n=k, cn=0.
Уравнение работы изменения объема, совершаемой телом при политропном процессе, имеет аналогичный вид с уравнением работы в адиабатном процессе, т. е.
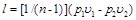 , (6.24)
, (6.24)
или

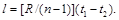 (6.25)
(6.25)
Изменение внутренней энергии газа и теплота в политропном процессе определяются по формулам:
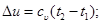
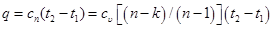 . (6.26)
. (6.26)
Изменение энтальпии в политропном процессе
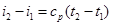 . (6.27)
. (6.27)
Изменение энтропии газа в политропном процессе определяется по формуле
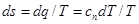 , (6.30)
, (6.30)
или для конечного изменения состояния
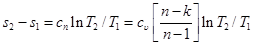 . (6.31)
. (6.31)
 2020-08-05
2020-08-05 4974
4974








