Международная ассоциация по изучению боли (IASP) определяет:
боль – неприятное ощущение и эмоциональное переживание, связанное с реальным или потенциальным повреждением ткани. Боль выполняет защитную функцию, являясь "сигналом" опасности.
Боль физиологична, пока информирует о повреждении. Как только сигнальная функция боли исчерпывается, она уже не нужна. Если болевые раздражения продолжают поступать в ЦНС, боль становится патологической, причиняет вред организму, постепенно нарушая его многие функции. Залог успешной борьбы с болью – понимание ее сущности.
Представления о механизмах появления боли были обобщены в 2-х основных теориях. Обе теории – две стороны единого целого.
1) Теория интенсивности (Goldscheider, 1894). Отрицается существование специальных болевых рецепторов. Боль могут вызвать разные достаточно сильные раздражители при стимуляции обычных сенсорных рецепторов (механо-, термо-, хемо-, фото-), если интенсивность стимуляции превосходит обычный уровень и достигает определенного критического уровня. Рецепторы генерируют импульсы, отличающиеся от импульсов при действии слабых раздражителей. Импульсацию распознает ЦНС, возникает ощущение боли.
В 1955 году характер такой импульсации пыталась объяснить теория распределения импульсов, или теория паттерна (англ. pattern – модель, устойчивая последовательность элементов): болевые стимулы вызывают особый порядок следования импульсов, отличный от разрядов, вызываемых другими раздражителями.
2) Теория специфичности противоположна теории интенсивности (M.Frey, 1894): признает существование специализированных болевых рецепторов – ноцицепторов (от лат. посеrе – повреждать и receptor – принимающий), которые отвечают только на интенсивные стимулы, возникающие при повреждающих воздействиях. Они составляют 25-40% всех рецепторов, расположены по всему телу, за исключением головного мозга и, возможно, костной ткани.
СТОМ Из тканей челюстно-лицевой области больше всего болевых рецепторов в тканях зуба. Так, на 1см2 дентина – 15 000-30 000 ноцицепторов, на границе пульпы и дентина – до 75 000, а на 1см2 кожи не более 200 болевых рецепторов. Выражена болевая чувствительностью у пульпы, её ноцицепторы с очень низким порогом чувствительности и их раздражение вызывает болевое ощущение исключительной силы.
3 типа рецепторов боли.
Первый тип – мономодальные (от лат. modus – способ), возбуждаются интенсивными механическими раздражениями (в меньшей степени термическими), поэтому их называют механоноцицепторами (илиА-δ-ноцицепторами – по типу нервных волокон). Порог для их стимулов выше нормального диапазона обычных механорецепторов, они активируются только сверхсильными раздражителями. Расположены преимущественно в коже, скелетных мышцах, фасциях, сухожилиях, суставных сумках, слизистых пищеварительного тракта.
Второй тип – полимодальные С-ноцицепторы (тельца безмиелиновых афферентных С-волокон) реагируют на механические, температурные и химические раздражения. Называют хемоноцицепторами, т.к. активируются 1) химическими веществами — алгогенами (высвобождаются при повреждении тканей и вызывают боль): тканевыми (серотонин, ацетилхолин, гистамин, простагландины Е2, F2α, D2, лейкотриены, избыток Н+, К+) и плазменными (брадикинин). Хемоноцицепторы расположены в коже и слизистых оболочках, во внутренних органах, где локализуются в стенках мелких артерий.
В развитии болевого сигнала также участвуют 2) медиаторы боли. Нейромедиаторы ноцицептивных афферентных волокон – глутаминовая и аспарагиновая аминокислоты. Но основной нейропередатчик – вещество Р (от англ. pain – боль). Оно действует в зоне формирования болевого импульса и на всех участках его передачи.Важное значение в формировании генераторов патологических возбуждений в структурах ЦНС, связанных с переработкой ноцицептивных возбуждений,имеет дефицит тормозных процессов, которые опосредуют глицин и γ-аминомасляная кислота.
Третий тип – так называемые " спящие" ноцицепторы, они активизируются только во время воспаления. Как и хемоноцицепторы, они представлены плотными некапсулированными гломерулярными тельцами С-волокон.
Общее для всех типов ноцицепторов:
1) активируются при действии раздражителей большой силы
2) изменчивость порога возбуждения. Величина порога чувствительности ноцицепторов зависит от многих факторов – их локализации, наследственных особенностей, эмоционального и соматического состояния организма.
На уровне задних рогов спинного мозга болевая афферентация подвергается начальному анализу и может быть даже заблокирована.
R. Melzack, P. Wall (1965) сформулировали теорию "входных ворот " – одну из наиболее плодотворных концепций механизмов боли. Основное научно-медицинское значение теории: в организме существуют специальные системы подавления боли, а спинной и головной мозг является активной системой, фильтрующей, отбирающей и воздействующей на входные сенсорные сигналы. Теория утвердила центральную нервную систему ведущим звеном в болевых процессах, в то время как теория специфичности отводила центральной нервной системе роль пассивного приёмника болевых импульсов.
Пути проведения ноцицептивной информации формируют 2 системы:
1) специфическую лемнисковую (спиноталамический тракт заднего столба спинного мозга)
2) неспецифическую экстралемнисковую (спиноретикулярный тракт).
Первая система представлена быстропроводящими А-волокнами и заканчивается в первой соматосенсорной зоне коры головного мозга, где формируется острая, точно локализованная боль. Её основная задача – обеспечить мозг немедленной информацией о наличии и степени повреждения, а также его локализации.
Вторая система представлена тонкими немиелинизированными С-волокнами, она проводит возбуждение к таламус у и второй соматосенсорной зоне коры больших полушарий. При этом возникает диффузная, постоянная боль, призванная ограничить активность поврежденного органа, а также формируются двигательные, вегетативные, эмоциональные реакции на боль.
Характер возникающих болевых ощущений зависит не только от состояния ноцицептивной системы организма, но и от антиноцицептивной системы – обеспечивает контроль за активностью структур, участвующих в восприятии, проведении и анализе болевых сигналов. В результате происходит торможение спинальных, стволовых, таламических нейронов, передающих импульсы от болевых рецепторов.
Антиноцицептивная система –
Это многокомпонентная эндогенная система подавления боли:
1) структуры спинного, ствола мозга и коры, прежде всего её второй соматосенсорные зоны, в которых формируются эфферентные ответы на болевые импульсы;
2) нервные пути, по которым из центральных нервных структур приходят эфферентные сигналы, возбуждающие выделение химических модуляторов в синаптических зонах и в местах формирования болевого сигнала;
3) нейромедиаторы – химические вещества различной природы, тропные к соответствующим рецепторам и обладающие способностью блокировать или модулировать (изменять) болевые импульсы;
4) рецепторный аппарат – различные типы рецепторов, на которые воздействуют разные нейромедиаторы для модуляции болевой информации.
В механизме ограничения болевого возбуждения участвуют системы мозга:
· серотонинергическая,
· норадренергическая,
· ГАМКергическая
· Опиоидергическая
Важнейшее значение отводится опиоидергической системе.
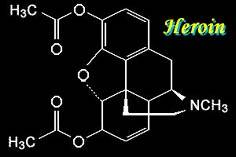
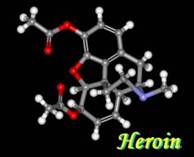
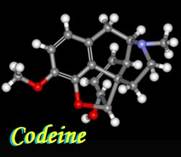
Термином «опиоиды» называют любые вещества (природные и синтетические), способные взаимодействовать с опиатными рецепторами (ОР). Все известные эндогенные опиоиды – пептиды. Их назвали опиоидными из-за способности связываться с теми же рецепторами, которые связывают морфин и другие опиаты.
По ХИМИЧЕСКОМУ СТРОЕНИЮ лиганды ОР бывают:
1). Алкалоидные (основной представитель – морфин – открыт в 1805 г.),
2). Пептидные (энкефалины, эндорфины, динорфины…).
Опиоидные рецепторы есть во всех областях спинного и головного мозга, участвующих в передаче болевой информации (желатинозная субстанция спинного мозга, гипоталамус, лимбические структуры и кора мозга, ретикулярная формация). Существуют 3 основных типа ОР — μ-(мю), κ- (каппа) и δ- (дельта) рецепторы, каждый из которых взаимодействует с определенными нейропептидами, в результате чего снижается болевая чувствительность.
Для связывания с опиатными рецепторами в составе реагирующей молекулы необходимо структурное присутствие хинолиновой кислоты, М.м=167,1 (пиридин-2,3-дикарбоновой – бензольное кольцо, где атом С1 заменен на N, а к атомам С2 и С3 присоединены кислотные (карбоновые) группировки).
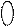
 –COOH
–COOH
–COОН
N Хинолиновая кислота
В процессе метаболизма этанола при полимеризации ацетальдегида с медиаторами образуются морфиноподобные продукты: бета-карболины,
тетрагидроизохинолины
В структуре опия (морфина) и ОП присутствует тирамин.
Структурные формулы и общая конфигурация активного центра, участвующего в связывании морфина, налоксона, опиоидных пептидов с ОР:



 НО HO
НО HO
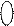 | 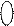 |
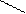
 _СН2–СН2–NH2
_СН2–СН2–NH2


 тирамин
тирамин




 О N–CН3 НО
О N–CН3 НО
 | |||
 | |||


 _СН2–СН–СО–ГЛИ–ГЛИ–ФЕН–МЕТ–ОН
_СН2–СН–СО–ГЛИ–ГЛИ–ФЕН–МЕТ–ОН
НО Морфин –ЛЕЙ–ОН
NH2 Мет(Лей)-энкефалин

 НО
НО
 |







 О ОН N–CН2–CН=CН2
О ОН N–CН2–CН=CН2
 |

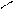 О Налоксон (налоксан)
О Налоксон (налоксан)
 |  |  |
В организме вырабатывается три группы эндогенных опиоидов – эндорфины, энкефалины и динорфины. Первыми были открыты энкефалины – два пентапептида мет-энкефалин и лей-энкефалин (остальные четыре аминокислоты одинаковые Тир-Гли-Гли-Фен-Мет/Лей). В гипоталамусе позже обнаружили более длинные (15-30 АК) опиоидные пептиды — α-, β-, γ- эндорфины, которые оказались в 12-100 раз активнее энкефалинов. Третья группа – динорфины. Опиоидные пептиды участвуют в обезболивании, в регуляции эмоциональных ответов, обладают антистрессорными свойствами, вырабатываются при мышечной работе. О пиоиды синтезируются не только в нервной ткани (в том числе локализованной в пульпе – в периферическом слое пульпы среди одонтобластов есть волокна, содержащие вещество Р), но и в надпочечниках, сердце (энкефалины). Особый интерес к этим соединениям и их синтетическим аналогам связан с надеждой найти анальгетики, к которым не возникает привыкания.
 2014-02-17
2014-02-17 776
776








