В результате изменения внешних параметров вещество может испытывать фазовый переход, т.е. переходить из одной фазы в другую через состояние равновесия фаз. При этом скачкообразно изменяются некоторые термодинамические функции. Если эти функции выражаются через первые производные термодинамических потенциалов, то такой переход называется фазовым переходом первого рода.
К фазовым переходам первого рода относятся: испарение (конденсация); плавление (кристаллизация); изменение кристаллической модификации. В этих переходах скачком изменяются удельный объем
 (12.1)
(12.1)
и удельная энтропия вещества
 . (12.2)
. (12.2)
Уравнение m1(P, T) = m2(P, T), определяющее условия равновесия фаз имеет своим решением функцию P = P (T), которая на диаграмме (P, T) изображается линией, называемой кривой равновесия фаз. Эта кривая разделяет области, в которых существует либо первая, либо вторая фаза вещества, а на самой кривой фазы находятся в равновесии. Например, кривая кипения разделяет жидкую и газообразную фазы, кривая плавления – твердую и жидкую, кривая возгонки (сублимации) – твердую и газообразную фазы вещества. Кривые равновесия фаз разделяют также различные кристаллические модификации вещества. (В действительности к кривой равновесия фаз примыкают достаточно узкие области метастабильных состояний, в которых вещество остается в исходной фазе и после перехода через кривую равновесия).
|
|
|
Так как в каждой точке кривой равновесия P = P (T) имеет место условие равновесия,
d m1= d m2. (12.3)
Дифференциал термодинамического потенциала Гиббса открытой системы G = N m = U + PV – TS равен
 . (12.4)
. (12.4)
Отсюда находим
 . (12.5)
. (12.5)
Поделив это равенство на число частиц, получаем приращение химического потенциала в виде
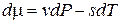 , (12.6)
, (12.6)
где v – удельный объем, а s – удельная энтропия вещества в расчете на молекулу.
На кривой равновесия фаз имеет место условие (3), которое с учетом равенства (6) можем записать в виде
 . (12.7)
. (12.7)
Отсюда получаем уравнение, определяющее наклон кривой равновесия фаз на PT -диаграмме:
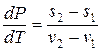 . (12.8)
. (12.8)
Оно называется уравнением Клапейрона-Клаузиуса. Со скачком удельной энтропии при фазовом переходе связана скрытая удельная (на молекулу) теплота перехода
 , (12.9)
, (12.9)
где T – температура перехода. Из этого определения видно, что скрытые теплоты прямого и обратного переходов отличаются знаком:  .
.
Подставив (9) в (8), приведем уравнение Клапейрона-Клаузиуса к виду
 . (12.10)
. (12.10)
При переходе вещества из жидкой или твердой фазы в газообразную скрытая теплота перехода и скачок удельного объема положительны для любого вещества, поэтому кривые кипения и возгонки имеют положительный наклон (dP / dT > 0). Для большинства веществ положительный наклон имеют и кривые плавления, но для таких аномальных веществ как лед, чугун и висмут кривая плавления имеет отрицательный наклон (dP / dT < 0).
|
|
|
Аномальные термодинамические свойства воды играют очень важную роль в природных явлениях. В частности, при затвердевании вода увеличивается в объеме, поэтому зимой водоемы замерзают с поверхности, а не со дна. Это предохраняет их от полного промерзания, так как теплопроводность льда из-за отсутствия конвекции значительно меньше чем у воды.
При увеличении давления температура плавления льда понижается. Хорошее скольжение коньков или санок по льду объясняется тем, что в точках контакта с поверхностью льда создается давление, которое обеспечивает его плавление и образование тонкой водяной пленки даже при температурах на десятки градусов ниже 0° С.
 2014-02-24
2014-02-24 2594
2594
