Лекция 9
Успехи фармакотерапии в значительной степени связывают не только с оптимизацией существующих, но и с разработкой принципиально новых лекарственных форм.
Среди последних внимание специалистов привлекают препараты с регулируемым (контролируемым) высвобождением лекарственных веществ - терапевтические системы, как их теперь называют в специальной литературе. Они обеспечивают длительное удерживание на постоянном уровне терапевтичес-кой концентрации лекарственных веществ в плазме крови и постоянство фармакологического эффекта. Таким образом, основная цель создания лекарственных форм с регулируемым высвобождением – это постоянно поддерживать заданный уровень концентрации лекарственного вещества в организме.
I. В зависимости от физического состояния матрицы – носителя терапевтические системы с регулируемым высво-бождением лекарственных веществ разделяют на:
1. Пленочные терапевтические системы.
2. Монолитные и не разрушающиеся в организме системы.
|
|
|
3. Монолитные биорастворимые (биоэродируемые) систе-мы.
4. Гидрогелевые терапевтические системы.
5. Осмотические мини- насосы.
II. По характеру основного процесса, определяющего скорость высвобождения лекарственных веществ, системы разделяют на:
1. Пассивные, у которых высвобождение лекарственных веществ идет вследствие диффузии в соответствии с градиентом концентрации (DС = С1-С2).
2. Активные, у которых высвобождение лекарственных веществ возникает под действием набухания носителя или его биодеструкции в организме.
3. В самостоятельную группу выделяют самопрограммирующиеся системы, высвобождение из которых происходит по эндосигналу, например, инсулинсодержащие системы, реагирующие на уровень глюкозы в крови.
III. С учетом пути введения терапевтических систем с регулируемым высвобождением разделяют на:
1. Пероральные.
2. Инъекционные.
3. Имплантируемые.
4. Чрескожные (трансдермальные).
5. Внутриполостные.
Доставка лекарственного вещества в заданную область организма происходит в несколько этапов:
1) высвобождение лекарственного вещества из системы;
2) его диффузия от поверхности системы в локальный кровоток;
3) транспортировка к соответствующему органу.
Достоинства: содержание лекарственного вещества в плазме крови после применения терапевтической системы с регулируемым высвобождением постоянно поддерживается на терапевтически обоснованном уровне, побочные действия снижаются или совсем исключаются, облегчается применение лекарственного средства, создается возможность приема лекарственных веществ с коротким периодом полураспада.
|
|
|
Недостатки:
I) высокая стоимость, сложность изготовления, возникно-вение новых продуктов при разрушении биодеструктируемых полимеров;
2) необходимость периодического вмешательства при введении и удалении имплантантов; болевые ощущения, вызванные присутствием имплантантов.
1.1. Мембранные пленочные терапевтические системы с пассивным механизмом (диффузионным) высвобождения
Разработаны системы с диффузионным механизмом высвобождения (резервуарные), ядро лекарственного вещества окружают полимерной пленочной оболочкой - мембраной. Контролируемое высвобождение лекарственных веществ достигается подбором соответствующей мембраны для конкретного лекарственного вещества. Учитывают проницае-мость мембраны для лекарственного вещества, размеры, однородность и извилистость пор, гидролипофильность и другие параметры мембраны.
Пример 1. Резервуарные мембранные системы для имплантаций под кожу или в мышечную ткань, представляют собой кольцо с внутренним диаметром 14 мм, наружным диаметром 20 мм из двух пленок. Эти две пленки разной толщины (0,014мм и 0,6 мм) из одинакового материала, соединены с помощью цианакрилатного клея, толщина всей системы 0,65мм. Устройство заполняется водной суспензией 5-фторурацила, высвобождение которого происходит только со стороны более тонкой пленки во времени.
Пример 2. Система "Oсusert " имеет эллипсовидную форму, площадь поверхности 5,5х13 мм, толщину 0,3-0,5 мм. Конструкция системы основана на том, что носитель лекарственного вещества заключен между двумя этиленвинил-ацетатными мембранами, регулирующими скорость высво-бождения лекарственного вещества. Мембраны соединены по краям жестким кольцом, окрашенным ТiO2, что позволяет видеть контур системы при введении в жидкие среды. Носитель пилокарпина представляет собой овальную пластину, которую получают растворением пилокарпина гидрохлорида в геле альгиновой кислоты с последующим высушиванием (на подложке) при пониженном давлении и температуре 30°С. Системы "Oсusert " обеспечивают
К достоинствам системы "Oсusert" следует отнести точность дозированного высвобождения пилокарпина, которое колеблется во времени в пределах ±20%. Система не изменяет рН слезной жидкости, обеспечивает стабильное гипотензивное действие пилокарпина в течение 7 дней.
Недостатки: сложность введения и извлечения системы, дискомфорт при использовании, дороговизна системы.
1.2. Монолитные (матричные) терапевтические системы
Монолитные (матричные) терапевтические системы разделяют на:
а) неразрушаемые;
б) биодеструктирующие в организме.
а). В первом случае система представляет собой раствор или суспензию лекарственного вещества в матрице из полимера, нерастворимого в организме. В качестве полимеров используют: силиконовый каучук, сополимер этилена и винилового спирта, полиметилметакрилат и др. Системы такого типа изготовляют в форме шаров, стержней или изделий иной формы, которые вводят в полости организма или имплантируют под кожу. Высвобождение поисходит за счет диффузии из матрицы в течении до 100 суток.
|
|
|
Достоинства: простота их изготовления, обеспечение непрерывного высвобождения веществ с большой молекулярной массой, например, инсулина, ферментов, антител.
Недостаток: такие системы по окончании терапевтичес-кого действия необходимо извлекать из организма.
Пример 1. Готовые лекарственные формы (монолитные матричные системы) на основе сополимера этилена и винилацетата в виде матриц-пластин толщиной 0,3 мм и шариков с диаметром 2,2 и 3,2 мм для глазных целей с пилокарпином. Достоинства: не раздражают слизистую глаза, легко могут быть введены в глаз и извлечены из него.
Пример 2. Гентамициновые терапевтические системы Septopal представляют собой шарики из полиметилметакрилата, соединенные в цепи по 10, 30, 60 шариков. Диаметр шариков 7 мм и масса 0,2 г. Каждый шарик содержит 4,5 мг гентамицина и 20 мг двуокиси циркония. Применяется при лечении хронических воспалений костного мозга и костных тканей, а также инфекций мягких тканей.В течение 24 ч из шарика высвобождается 400-600 мкг гентамицина, 10 дней - 120 мкг, 20-дней - 50 мкг. Через 80 суток высвобождается по 10 мкг гентамицина в сутки.
б). Особый интерес представляют системы на основе биодеструктирующих носителей, позволяющих сочетать достоинства лекарственной формы типа Septopal с возможностью полного рассасывания таких систем в организме.
В качестве носителей, применяемых для получения биорастворимых систем, используют сополимеры акриламида и винилпирролидона и этилакрилата, на основе которого разработаны глазные лекарственные плeнки с лекарственными веществами различного действия: анестетиками, антибиотика-ми, противовирусными, сульфаниламидами, гипотензивными.
|
|
|
На основе биораствормых полимеров разработаны также лекарственные пленки для лечения гинекологических и стоматологических заболеваний. Для лечения и профилактики ишемической болезни предназначены пленки тринитролонг и динитросорбилонг, содержащие соответственно нитроглицерин и нитросорбит. В стадии клинических испытаний – инсулиносодержащие пленки для лечения диабета.
Биодеструктируемые полимеры применяют также для получения имплантантов в виде капсул, стержней, гранул, таблеток, шариков, пленок и др. К биодеструктирующим полимерам, применяемым в качестве носителей лекарственных веществ, относятся: полиамиды, полиуретаны, полиацетаты, полиортоэфиры, а также природные соединения: полисахариды, производные амилозы и декстрана, протеины, коллаген, альбумин.
Биодеструктирующиее полимеры являются перспективны-ми носителями различных фармакологических групп: контрацептивов (прогестерон, норгестрен), противоалкогольных (антабус), противомалярийных, противодиабетических (инсулин), противоопухолевых (циклофосфамид), анестетиков (дибукаин), антибиотиков и др.
1.3. Терапевтические гидрогелевые системы
Гидрогели используют при изготовлении глазных контактных линз, которые можно рассматривать в качестве перспективных систем для контролируемого высвобождения лекарственных веществ. С этой целью применяют сополимер оксиэтиленметакрилата, который импрегнируют различными лекарственными веществами: противоглаукомными, антибио-тиками, витаминами и др.
Применяют также полиэтиленоксидные - поперечно сшитые молекулы, которые образуют каучукоподобные гидрогели, обладающие механической прочностью. Включение лекарственных веществ в такую полиэтиленоксидную матрицу осуществляется простым гидратированием геля в растворе лекарственного вещества.
Созданы и апробированы в клинической акушерской практике вагинальные пессарии на основе поперечно сшитого полиэтиленоксида – гидрогеля, содержащего простагландин Е2, который обеспечивает равномерное высвобождение последнего в течение 24 часов. Другим преимуществом этой системы является возможность стабилизировать простагландины, которые в свободном состоянии имеют очень краткий период биологического полураспада.
Хотя гидрогели могут вводиться в организм различными способами, предпочтение следует отдать вагинальному и ректальному использованию таковых.
Предложены гидрогели на основе сополимеров оксиэтилметакрилата и этиленгликольдиметакрилата. Введение лекарственных веществ осуществляется в такой гидрогель непосредственно при полимеризации или насыщением гидрогеля водными растворами лекарственных веществ.
Пероральные гидрогели на указанном полимере с прокаинамидом имеют преимущество перед обычными тверды-ми капсулами с этим веществом – пролонгированное высвобождение, так как коэффициент диффузии прокаинамида из гидрогеля с увеличением концентрации сшивающего агента (полимер 2-оксиэтилметакрилат) уменьшается в 20 раз.
1.4. Осмотические мини-насосы
Пример 1. Для обеспечения длительного и равномерного высвобождения стероидов предлагается лекарственная форма "капсула в капсуле"(рис 9.1), в которой 7,9 мг кристаллического стероида, помещены в капсулу, внутренний диаметр которой составляет 1,57 мм, длина - 5 мм. Капсула изготовлена из диметилполисилоксана и помещена в свою очередь в наружную капсулу.
Пространство между емкостью со стероидом (внутренней капсулой) и стенками наружной капсулы заполнено физиологическим раствором. Форма "капсула в капсуле" обеспечивает длительное и постоянное высвобождение стероида, причем начальная скорость этого процесса значительно ниже, чем в контрольном образце стероида, заключенного только в капсулу. Обращено внимание на роль физиологического раствора в создании постоянства градиента концентрации стероида. Скорость выделения последнего возрастает с увеличением поверхности внутренней емкости.
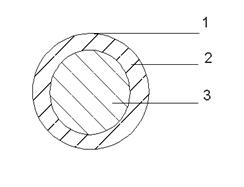 Рисунок 9.1
Рисунок 9.1
Схема пероральной системы «капсула в капсуле»
1 – стенка наружной капсулы,
2 – физиологический раствор,
3 – внутренняя капсула.
Пример 2. Пероральная терапевтическая система "Орос" (рис. 9.2) представляет собой покрытую оболочкой таблетку, которая состоит из осмотического ядра, полупроницаемой мембраны из ацетата целлюлозы и небольшого отверстия в мембране.
 2014-02-24
2014-02-24 5263
5263
