Количественный анализ Распределение световых потоков при прохождении возбуждающего излучения через люминесцирующий раствор
В основе количественного анализа лежит зависимость интенсивности люминесценции от концентрации люминесцирующего вещества где К – коэффициент пропорциональности В кв – квантовый выход люминесценции I 0 – интенсивность возбуждающего света ε - молярный коэффициент поглощения l – толщина слоя раствора Это соотношение справедливо, если постоянны: квантовый выход интенсивность возбуждающего света
Зависимость линейна в пределах 3-4 порядков величин концентрации (10 -7 -10 -4 М) При концентрациях >10 -4 М линейность графика нарушается из - за концентрационного тушения люминесценции, самопоглощения и др. Зависимость интенсивности флуоресценции от концентрации флуоресцирующего вещества
Определение органических соединений основано на а) прямых методах по флуо - и фосфоресценции б) эффекте Шпольского в) фосфоресценции при комнатной температуре Эффект Шпольского – возникновение квазилинейчатых спектров люминесценции и поглощения в специально подобранных растворителях, размеры молекул которых совпадают с размерами молекул люминофора при низких температурах При этом молекулы изолированы друг от друга и жестко закреплены в растворителе, вследствие чего спектры представляют собой серию узких спектральных линий и обладают ярко выраженной индивидуальностью
|
|
|
53. Химическая связь в органических соединениях. σ пи и τ связи. Водородная связь. Донорно-акцепторная связь
Ионная –связь, осуществляемая за счет электростатического притяжения м/у ионами с зарядами противоположного знака.
Ковалентная – связь, осуществляемая взаимодействием двух электронов, принадлежащих до образования разным атомам, в рез-те вз-ия образуется общая электронная пара.
σ- связь –ков. связь, обладающая круговой симметрией.
π-связь – ков. связь, образованная перекрыванием двух р-орбиталей, главные оси которых параллельны.
τ-связь - связь С-С, в которой отсутствует круговая симметрия, "банановая связь", т.е. не достигается максимальное перекрывание атомных орбиталей.

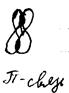
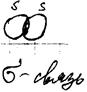
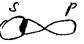

Водородная связь - связь, когда атом водорода связан с электроотрицательным атомом, который смещает на себя электронное облако, создавая тем самым полож. заряд на водороде.
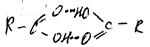
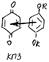
Донорноакцепторная – связь образуется при вз-ии атома с неподеленной электронной парой и атома с незаполненной внешней электронной оболочкой.
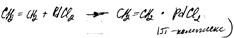
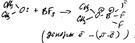
 2015-08-12
2015-08-12 946
946








