Дициклические
Их делят на 4гр., в зависимости от входящих УВ.
 |  |  |  | ||||
Туйан каран пинан камфан
α-Пинен
 |  |
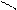

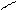
 или
или
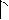 | 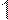 |
Содерж.в различ.эфирных маслах, но наиб.кол-во содеж-ся(до 75%) в скипидаре.
Скипидар получают перегонкой с водяным паром живицы(хвойные деревья), неперегоняемый остаток наз-ся конифолью.
Очищ.скипидар в технике исп-ся как р-пь, а в медицине для втирания в кожу, как раздраж.в-во.
Намиб.применение α-пинена-для получ.терпингидрата и камфоры.
Получение терпингидрата:
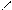



 OH
OH

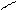
 + 3H2O H2SO4
+ 3H2O H2SO4

 Длит.время *2H2O
Длит.время *2H2O


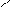
 OH
OH
Производные камфана:
Эти спирты могут превращ.взаимно друг с друглм при кипяч.с Na мет.
Спирты

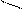


 OH - борнеол
OH - борнеол

 H
H
Терпингидрат

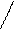
 H - изоборнеол
H - изоборнеол

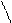 OH
OH
Диантиомеры и рацематы содерж.в раст.в свободном виде, так и в виде
(-)левовращ.-в эфиро-пихтовых маслах.
(+)правовращ.
Борнеолы проявл.св-ва втор.спиртов при их окисл.обр-ся камфора.

 *
*
=O

Комфора содерж.в эфир.маслах камфорного дерева, с др.вр.исп-ся для стимуляции сердеч.деятельности.
2 хир.центра, 2 энантиомера:




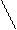

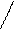
 =O O=
=O O=





Особенности:
1) в молек.2 ассиметр.атома С, но вместо 4-х изомеров известно 2, что связано с жестк.системы, конфигурации обеих хир.центров изменяется одновременно.
2)шестичн.кольцо в пр-ве занимает комформ-ванну синтез комфоры из α-пирена по Тищенко:
 |  |  |  | ||||||||
 |  | ||||||||||


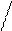
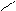

 TiO2*H2O CH3COOH OCOCH3
TiO2*H2O CH3COOH OCOCH3
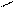

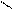






 180
180
 |  |
Камф-ен (очень бормилацитал
реакц.спосб)
 | |||
 |

 H2O OH [O] =O
H2O OH [O] =O
 -CH3COOH
-CH3COOH
Бормеол
Хим.реакц.многих терпенов сложны и часто сопровожд.перегруппир.скелета.
Гидрохлорирование пинена приводит к борнилхлориду.



 +
+






 +H+ перегруп-ка + +Сl- Cl
+H+ перегруп-ка + +Сl- Cl
 |  |  | |||||||||||
 | 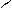 | ||||||||||||
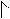 | 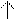 | ||||||||||||
Третичный катион II борнилхлорид
Карбокатион I более устойчив
Чем карбокатион I
По хим.св-ам типичный кетон (все реак.AN, присоед.-отщеп.аксимы, гидразоны, фенилгидразон), кроме того метиленовая гр.в α-полож.проявл. CH-кисл.св-ва.
 | |||
 |

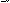 =O +Br2 =O + HBr
=O +Br2 =O + HBr
 C-H Br
C-H Br
H бромкасфона
Улучш.серд.деятельность.
 2014-02-02
2014-02-02 670
670








